Mini células que curam: método inovador propõe uso sustentável de plaquetas sanguíneas em terapia celular e medicina regenerativa
Autoras: Sheila Siqueira Andrade e Alessandra Valéria de Sousa Faria
Plaquetas são peça-chave no processo de cicatrização e regeneração da maioria dos tecidos do corpo. O problema é a dificuldade de armazenamento, que leva ao desperdício e descarte de grande quantidade desse precioso hemoderivado.
O grande desafio atual da Biotecnologia é fornecer soluções aplicadas à medicina e à saúde, recriadas em laboratório com um padrão próximo ao que ocorre em nosso organismo. Seguindo os conceitos de Biomimetismo (imitação da vida), a PlateInnove Biotechnology, uma startup brasileira resolveu inovar e desenvolveu projetos na área de bioativação de “minicélulas” (plaquetas) sanguíneas humanas. Através do desenvolvimento de uma plataforma biotecnológica, na qual plaquetas (matéria-prima) são seletivamente bioativadas para a produção de um painel de fatores de crescimento customizados destinados às áreas de pesquisa e desenvolvimento, veterinária e cosmética.
Desmistificando as Plaquetas
O processo de cicatrização de uma “pequena” ferida não é algo marcante que fique na memória. É provável que a maioria das pessoas não se lembre da última vez que sofreu um pequeno corte. Talvez algumas sensações sejam associadas ao evento como uma dor inesperada, uma pontada aguda e a imediata visão de sangue saindo lentamente da ferida. O primeiro instinto é proteger a ferida com um pequeno curativo a fim de interromper a perda de sangue. Mas sem preocupação. E porque agimos naturalmente diante desse sangramento, sem tentar descobrir como e quando esse sangramento vai parar? A resposta é simples, sabemos que nosso corpo cuidará disso. A razão pela qual não sangraremos até a morte, toda vez que nos cortamos, se deve principalmente a minicélulas do nosso sangue chamadas plaquetas (figura 1).
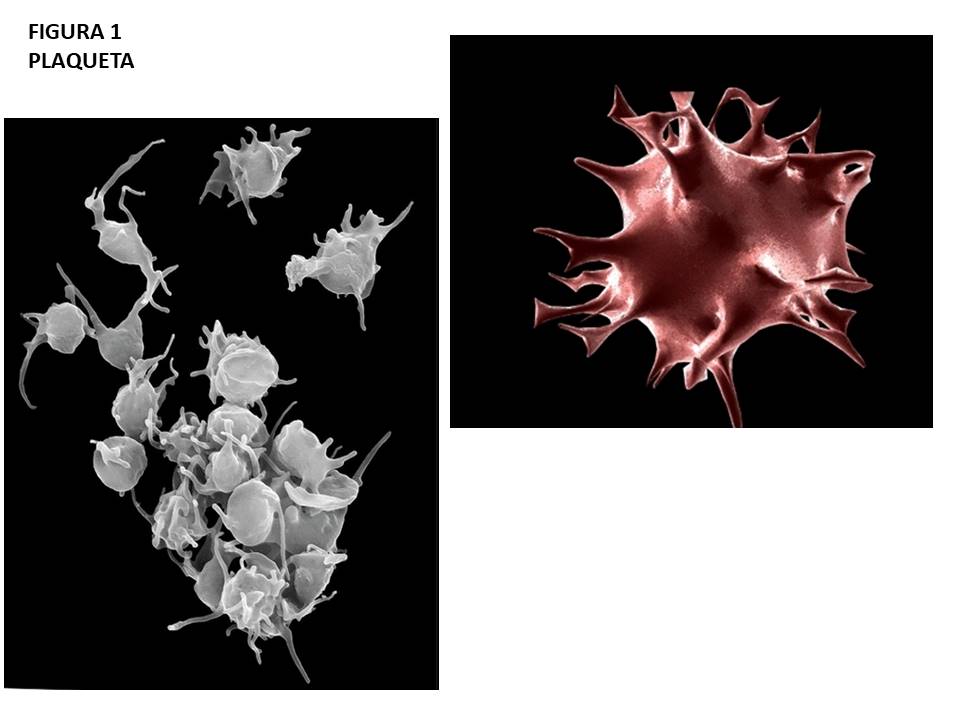
Nosso sangue é composto por diferentes tipos de células suspensas num fluído denominado plasma. Dentre essas células destacamos as plaquetas, células (anucleadas), de ontogênese fragmentária (a partir de sua célula progenitora, megacariócito), em formato de disco, extremamente pequenas (1 a 2 μm), produzidas na medula óssea e no pulmão, que circulam no sangue em seu estado de repouso.(1,2) Em uma pessoa saudável encontramos de 150 a 300 mil plaquetas (por microlitro de sangue) circulando na corrente sanguínea, por até 10 dias (seu tempo de vida útil).(3) Como protagonistas da coagulação do sangue (mantenedoras da integridade de vasos sanguíneos impedindo sangramentos) e altamente especializadas, essas “minicélulas” transitam em processos dinâmicos e cruciais para a manutenção do equilíbrio do nosso organismo, como o processo inflamatório e sistema imunológico. Por ser uma “minicélula” especializada, é de sua responsabilidade a primeira avaliação e os primeiros reparos no tecido lesionado. Ou seja, plaquetas são “soldados de fronte de batalha”. Carregam em seu interior uma vasta quantidade de compartimentos/organelas e grânulos (α -alfa e denso) responsáveis pelo estoque de moléculas e íons (cálcio e magnésio) biologicamente influentes. No interior dos grânulos α não estão apenas fatores de coagulação do sangue, mas também compostos efetores como fatores de crescimento, mensageiros do sistema imune e enzimas, importantes por controlar situações difíceis, como um corte simples ou mesmo um dano tecidual extenso.(3) Em resposta ao corte/ferimento o organismo envia sinais de alerta através da corrente sanguínea, notificando as plaquetas do trauma. Sendo as “primeiras” células a chegarem ao local da lesão, as plaquetas são ativadas com consequente liberação seletiva dos mediadores de seus compartimentos, recrutando outras plaquetas nas proximidades e iniciando a sua mudança de forma, de estado de repouso/quiescente no formato de “disco” para uma forma “estelar”, sua forma ativada com formação de pseudópodes.(4,5)
O recrutamento de outras plaquetas é facilitado pelo fato de sua superfície ser preenchida por estruturas que servem como identificadores/biossensores/receptores aos fatores plaquetários liberados neste processo, um processo de reconhecimento entre plaquetas. Isso as ajuda a ficar unidas. Essa união é conhecida como agregação plaquetária que envolve inúmeras plaquetas. Ao mesmo tempo, outros fatores de coagulação estão em ação. Uma proteína no sangue chamada fibrinogênio se torna ativa também. E uma vez ativa, essa proteína recebe o nome de fibrina e, como o próprio nome sugere, produz fibras que atuam em conjunto com as plaquetas. Essas fibras cobrem a ferida e criam uma rede e, portanto, menos sangue pode escapar. No entanto, as plaquetas ainda precisam terminar seu trabalho, com a formação de um agregado plaquetário contendo glóbulos vermelhos que funciona como um “tampão” (curativo), um coágulo, impedindo a perda de sangue (figura 2).(4-6)
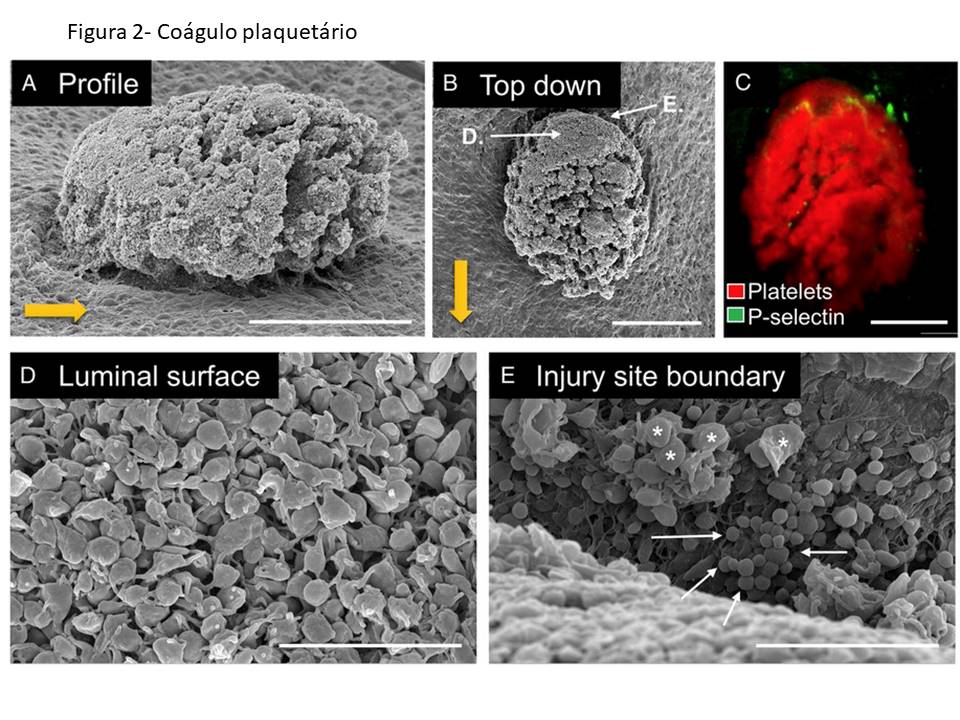
Ainda no local da lesão, as plaquetas iniciam o recrutamento de outros tipos celulares, onde a liberação de seus fatores de crescimento internos é novamente crucial. Uma vez liberados, os fatores de crescimento plaquetários atuam como guias (quimiotáticos) e suplemento nutritivo para células como monócitos/macrófagos(6)*, granulócitos, fibroblastos, epiteliais e até as próprias células do vaso sanguíneo. E assim, sem perda de sangue, inicia-se o processo de cicatrização da ferida, e regeneração do tecido.
Uso off label do concentrado de plaquetas
Como se vê, a plaqueta é peça crucial em nosso organismo, por fazer parte da maquinaria da coagulação do sangue, e por isso estão sempre em alta demanda. Pacientes que sofreram traumas (e que perderam muito sangue), em tratamentos quimioterápicos e submetidos à cirurgia, muitas vezes precisam de transfusões de plaquetas para manter o sangue funcionando adequadamente. O mesmo acontece com as pessoas com distúrbios genéticos, que as impedem de produzir plaquetas suficientes por conta própria, causando baixa contagem de plaquetas (trombocitopenia). Como consequência, aparecem sangramentos espontâneos e um pequeno corte pode se tornar algo mais grave. No entanto, as plaquetas são escassas em comparação aos outros produtos sanguíneos, em parte devido à sua curta vida útil.
Nos bancos de sangue, os glóbulos vermelhos podem ser armazenados em refrigerador (4°C) por 42 dias, e o plasma pode ser congelado (-80°C) por anos. No entanto, plaquetas precisam ser armazenadas à temperatura ambiente (22°C) sob leve agitação, e apenas por um curto período (5 dias), devido à grande probabilidade de contaminação bacteriana. O que significa que poucas plaquetas estão disponíveis para aqueles que precisam delas. Essa situação é contraditória, porque apesar de faltar plaquetas para transfusão, há também perda expressiva por vencimento do prazo de validade. Cerca de 20% das unidades de plaquetas produzidas nos bancos de sangue acabam virando lixo/resíduo biológico, por não estarem viáveis para as práticas hemoterápicas. Neste cenário, PlateInnove Biotechnology surge em 2017 com a proposta de aproveitar esse nobre material de maneira segura, estruturando um negócio de impacto biotecnológico, social e ambiental. Com uma plataforma de bioativação de plaquetas (matéria-prima) gera-se uma produção customizada de proteínas de alto valor biológico e de alto valor agregado destinadas às áreas de pesquisa e desenvolvimento, veterinária e cosmética. Dentro do atual panorama brasileiro de empreendedorismo, a start-up segue alinhada com as recomendações sinalizadas pela Organização Mundial de Saúde(9) (OMS, do inglês WHO, World Health Organization), que propõem o reaproveitamento racional das unidades de plaquetas.
Obtenção das Plaquetas
As unidades de plaquetas foram obtidas dos serviços do Hemocentro de Campinas/UNICAMP, do Hemocentro de Ribeirão Preto/USP e da COLSAN (Associação Beneficente de Coleta de Sangue). E como os bancos de sangue produzem as unidades de plaquetas? A partir do sangue total doado por voluntários, os bancos de sangue processam o sangue para a produção das unidades de plaquetas majoritariamente por uma técnica denominada “buffy coat” e minoritariamente por “PRP” (plasma rico em plaquetas). Do restante do sangue também são produzidas as unidades/bolsas de hemácias, plasma e o crioprecipitado. Para a plataforma, utilizamos as unidades de plaquetas do quinto dia de processamento, já expiradas. O projeto de pesquisa tem a aprovação do comitê de ética, via plataforma Brasil, o apoio da FAPESP (Fundação de Amparo a Pesquisa do Estado de São Paulo) e aprovação pelas comissões de pesquisa dos Hemocentros parceiros.
Vale ressaltar que devido as especificações de aplicações finais dos produtos, as unidades de plaquetas são manipuladas em capela de fluxo de ar laminar devidamente instalada em laboratório apropriado para o cultivo de células, seguindo as normas de biossegurança.
Como analisar o que não enxergamos? Ativação de Plaquetas por Citometria de Fluxo
Para certificar o grau de pureza e integridade das preparações de plaquetas, utilizamos a técnica de citometria de fluxo para
- separação de células ativadas através de uso de sondas;
- quantificação da porcentagem de células contaminantes;
- separação de uma população celular pela complexidade.
O equipamento utilizado* consiste em um conjunto de lasers e conexões para manter as análises de amostras líquidas em fluxo. Utilizamos para esse ensaio um anticorpo para estruturas proteicas presentes somente na superfície de plaquetas, o anti-CD61 ligado a uma sonda fluorescente/brilhante FITC. Deste modo, quando a suspensão de plaquetas (amostra) passar em fluxo pelas conexões do equipamento o laser discriminará pela fluorescência o que é plaqueta e o que não é, bem como a concentração e a complexidade/ativação das “minicélulas”. Sabendo que as plaquetas mudam de sua forma “disco” para uma forma “estelar” (quando expostas a estímulos na corrente sanguínea), adicionamos a solução uma proteína, Anexina-V, ligada a outra sonda fluorescente PE que indicará a mudança de forma da plaqueta.
Detectando a luz das “minicélulas”? – Visualizando Plaquetas por Microscopia de Fluorescência
Utilizar a microscopia de fluorescência nos permite iluminar componentes específicos das células como as plaquetas, e analisar intimamente processos poucos explorados. Através de sondas fluorescentes (sondas que brilham/iluminam quando estimuladas por um laser), a técnica revela detalhes do funcionamento das plaquetas sem destruí-las, mantendo-as vivas. Assim podemos analisar de maneira criteriosa processos que envolvam a liberação e/ou produção dos fatores plaquetários, no nosso caso os fatores de crescimento.
A Biomodulação de Plaquetas – Plataforma PlateInnove Biotechnology
Uma vez validadas nossas “provas de conceito” conduzimos para o teste de efetividade da plataforma, com a execução da bioativação das “minicélulas”. Este é um processo que se encontra em pedido de registro de patente (INPI PCT – BR 10 2017 017952 4) e em parte também é mantido em sigilo industrial, porém podemos expor que a bioativação de plaquetas segue o conceito do biomimetismo (do grego bio – vida; miméticos – imitação). E o que seria esse conceito? Biomimetismo é uma área da ciência que procura explorar e aprender com a natureza, sobre suas estratégias e soluções, e utilizar esse conhecimento para resolver problemas humanos. No nosso caso, seguimos o racional “pergunte ao nosso organismo”, onde a bioativação de plaquetas em laboratório, induz a produção customizada e racional de fatores de crescimentos plaquetários envolvidos nos processos de reparo de feridas e regeneração tecidual.
Controle de qualidade de matéria-prima: os Resultados de uma Análise em Fluxo
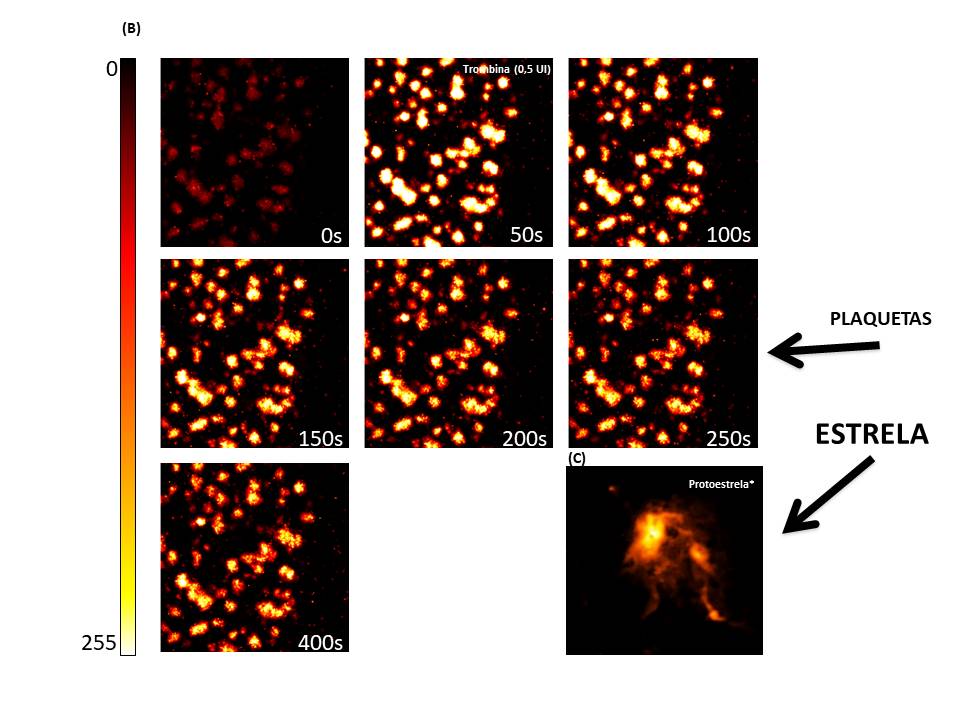
Uma vez que as plaquetas apresentam ação crucial para o contingenciamento do sangramento, a primeira análise avalia a capacidade das plaquetas provenientes dos bancos de sangue de responderem a estímulos químicos, similares ao que acontece na corrente sanguínea, imediatamente a um ferimento. As plaquetas (presentes nas bolsas) se encontram em repouso (forma de disco), no entanto, após estímulo, adquire sua forma ativada, forma “estelar”. Essa mudança de forma é detectada pelo equipamento citômetro de fluxo com as plaquetas em movimento. Com esses resultados garantimos que a matéria-prima (suspensão de plaquetas) seja homogênea, identificamos o número de plaquetas real da solução e certificamos que as plaquetas estejam responsivas à bioativação seletiva para produção de proteínas de alto valor biológico.
Validação do controle de qualidade de matéria-prima: onde há Luz há um Fator Plaquetário
Seguindo o raciocínio, “plaquetas em ação”, agora analisamos as plaquetas internamente. Como são as menores células circulantes em nosso sangue, as plaquetas só podem ser vistas em detalhes com o uso de um microscópio de alta resolução. E ao analisá-las intimamente utilizando sondas fluorescentes, somos não somente presenteados com belas imagens, mas também obtemos dados confiáveis. Para isso, acompanhamos a plaqueta desde a sua ativação com a mudança de forma, até o momento em que seu conteúdo interno é esgotado.
Curiosidade: O sangue que nos envolve e o céu que nos abraça
Antes de compreender o que é uma estrela, a criança aprende a identificar/reconhecer pequenos pontos luminosos no céu. Logo, identifica no céu as estrelas, o sol e a Lua. Porém, a criança não tem a mesma percepção lúdica, em relação ao seu primeiro machucado. Por questões óbvias, não enxergamos nossas células agindo a “olho nu”. Muito menos conseguimos fazer um paralelo de que pequenas células no formato de estrelas são as responsáveis pela cicatrização de uma ferida. Mas um pesquisador israelense9 conseguiu correlacionar os mecanismos básicos que permeiam o cosmo do sistema biológico. Ele descreve que uma estrela como o sol (uma célula multipotente) pode diferenciar-se em planetas ricos em metais como a Terra e pobres em metais como Júpiter. Mas de maneira alternativa, essa mesma estrela (o Sol) pode se fragmentar e formar os mesmos planetas. E esse fenômeno de fragmentação celular em modelos biológicos está relacionado a fragmentação de células mãe precursoras das plaquetas, os megacariócitos. Sua fragmentação pode gerar milhares de plaquetas de uma vez. Não é por acaso que essas “minicélulas” adquirem uma forma estelar quando ativadas. *Vale lembrar que esse é um processo minoritário, uma vez que a grande maioria das células são produzidas pelo processo de divisão celular.
Análise em Fluxo ou Imagem com Fluorescência?
Em se tratando da análise detalhada e efetiva das plaquetas precisamos explorar, planejar e nos beneficiar das tecnologias mais avançadas, uma vez que são ferramentas aliadas a inovação. Selecionar técnicas que nos auxilie na validação da produção customizada de fatores de crescimento é poder acelerar o processo de inovação, desenvolvimento e materialização de uma ideia. As duas tecnologias podem ser complementares se o objetivo for à comprovação de um resultado e consequente validação de um processo. E é justamente sobre validação de processo que estamos falando. As duas técnicas ilustradas aqui serviram de base para refinar o desenho funcional da plataforma, permitindo checar a qualidade da matéria-prima. Tanto a citometria de fluxo quanto a microscopia de fluorescência forneceram informações que demonstraram a qualidade da matéria-prima utilizada, uma garantia que a plataforma irá executar de maneira eficiente a bioativação das plaquetas para produção rápida de proteínas de alto valor biológico.
A Efetividade da Plataforma PlateInnove – Bioativação de “Minicélulas”
Diante da integração dos resultados obtidos até aqui, o desenho da plataforma de bioativação de plaquetas seguiu de maneira eficiente. Como explorado neste artigo, a participação das plaquetas nos processos de coagulação sanguínea, cicatrização e regeneração tecidual é crucial. Elas orquestram respostas biológicas complexas durante toda a vida humana, fornecendo seus fatores plaquetários como solução sincronizada e efetiva. E transpor toda essa complexidade multifatorial e multifuncional para uma plataforma, só foi possível aplicando o conceito do biomimetismo. A manipulação coordenada das “minicélulas” explorando seu programa biológico já preexistente permite a produção de um conjunto seletivo de fatores de crescimento. E qual o racional por trás dessa tecnologia?
Obter fatores de crescimento biomiméticos, ou seja, com 100% de similaridade com o que é encontrado no organismo humano. Ineditismo, a plataforma é capaz de produzir um “burst” seletivo de fatores de crescimento, porém de maneira natural, ou seja, utilizando a fábrica natural (as plaquetas) destas moléculas.(3) Características que dão ao produto, o InGrowth®, desenvolvido pela PlateInnove Biotechnology um grande diferencial frente aos fatores de crescimento sintéticos (proteínas recombinantesh) já produzidos e inseridos no mercado.
Na figura 3 ilustramos a sequência de processos da plataforma para obtenção do InGrowth® contendo fatores de crescimento plaquetários relacionados, por exemplo, ao processo de neovascularização, denominado angiogênese. E para ilustrar a capacidade das plaquetas de estimularem as células de vasos sanguíneos (células endoteliais) a se organizarem em estruturas tubulares, utilizamos o sistema de monocultura de células em camadas (suportes) biomiméticas. E como funciona esse sistema? Esse sistema consiste em estimular o crescimento através do crosstalk (conversa) entre fatores proteicos derivados das plaquetas e células específicas. Em outras palavras, a PlateInnove Biotechnology desenvolveu o InGrowth® aditivado com fibrinogênio (InGrowth®Bio enriquecido com fibrinogênio) que garante ao mesmo tempo estímulo para as células se multiplicarem (divisão celular estimulada por fatores de crescimento) e suporte (fibrina), propiciando que as células endoteliais se organizem e formem estruturas tubulares, angiogênicas, (como o formato de canículas do vasos sanguíneos).
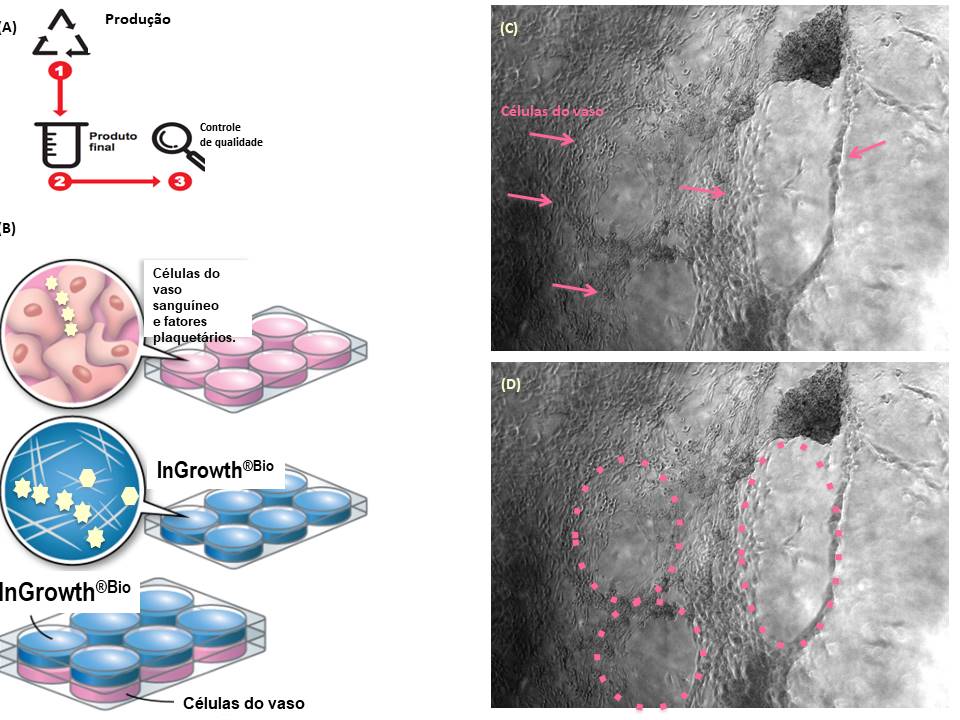
Na figura 4 temos a imagem obtida por microscópio de luz invertido, de células endoteliais se organizando em estruturas tubulares. Essa organização foi favorecida pela interação das células endoteliais com os fatores plaquetários, sobre o suporte/molde de fibrina. Esses fatores de crescimento (PDGF, VEGF e FGF) fornecem estímulos direcionados à células endoteliais. Na figura 4D, a mesma imagem explorada na figura 4C, agora indica as estruturas angiogênicas (na cor amarela) formadas pela organização das células endoteliais estimuladas pelos fatores de crescimento plaquetários e amparadas pelos feixes/fibras de fibrina. Um sistema de co-cultura biomimético e humanizado.
Diante dos resultados discutidos no artigo e dos avanços nos processos de inovação da PlateInnove Biotechnology, a plataforma desenvolvida pela startup permite, em laboratório, manipular plaquetas com um padrão próximo ao que ocorre em nosso organismo, gerando proteínas chaves para os processos de cicatrização e regeneração tecidual. Criando um cenário tripartite: científico, ambiental e social. Uma “biotecnologia sustentável”, agregando valor científico e tecnológico a um subproduto nobre, entregando modelos biotecnológicos inovadores.
Agradecimentos
À equipe da PlateInnove Biotechnology (Katia Ferreira e Cristiane Siqueira Taxa Ribeiro). Aos bancos de sangue parceiros: o Hemocentro de Campinas/UNICAMP, o Hemocentro de Ribeirão Preto/USP e COLSAN. À FAPESP (Fundação de Amparo a Pesquisa do Estado de São Paulo) Programa de Pesquisa Inovativa em Pequenas Empresas (PIPE) Fases 1 e 2, Processos 2016/14459-3 e 2017/26317-1.
Autoras:


Referências Bibliográficas
- Machlus KR; Italiano JEJr. The incredible journey: from megakaryocyte development to platelet formation. Journal of Cell Biology. 2013;v.201, p. 785–796. doi: 10.1083/jcb.201304054.
- Lefrançais E, Ortiz-Muñoz G, Caudrillier A, Mallavia B, Liu FC, et al. The lung is a site of platelet biogenesis and a reservoir for haematopoietic progenitors. Nature. 2017; v.544, n. 7648, p. 105-109. doi: 10.1038/nature21706.
- Andrade SS, de Sousa Faria AV, de Paulo Queluz D, Ferreira-Halder CV. Platelets as a ‘natural factory’ for growth factor production that sustains normal (and pathological) cell biology. Biol Chem. 2020; 401(4):471–476. doi:10.1515/hsz-2019-0342
- Semple J, Italiano J, Freedman J. Platelets and the immune continuum. Nature Reviwes Immunology. 2011;v. 11, p. 264–274. doi: 10.1038/nri2956.
- Oliveira I, Girão M, Sampaio M, Oliva ML, Andrade SS. Plaquetas: Papéis tradicionais e não tradicionais na hemostasia, na inflamação e no câncer. Arquivos Brasileiros da Ciência e Saúde (ABCS) Health Sciences. 2013;v. 38, p. 153-161.
- Andrade SS, Sumikawa JT, Castro ED, Batista FP, Paredes-Gamero E, Oliveira LC, et al. Interface between breast cancer cells and the tumor microenvironment using platelet-rich plasma to promote tumor angiogenesis – influence of platelets and fibrin bundles on the behavior of breast tumor cells. Oncotarget. 2017; v. 10, p. 16851-16874. doi 10.18632/oncotarget.15170.
- Weinberg RA. The Biology of Cancer. 2 ed. New York: Garland Science, 2014.
- WHO guidelines on tissue infectivity distribution in transmissible spongiform encephalopathies. Geneva, Switzerland, 2006. Disponível em: <https://www.who.int/bloodproducts/en/>. Acesso em: 05 jun. 2019.
- Kleinmann R. Similarities between basic mechanisms of cosmic and biologic systems. International Journal of Physical Sciences. 2015;v. 11, p. 01-10. doi.org/10.5897/IJPS2015.4396.
- ALMA (Atacama Large Millimeter/submillimeter Array), <https://www.eso.org/public/portugal/images/potw1712a/>. Acesso em: 10 mar. 20
Ainda sobre medicina regenerativa, vocês cientistas poderiam iniciar uma pesquisa usando a medicina regenerativa para desenvolver alguns órgãos humanos como por exemplo ( pênis) que um medico cientista já está desenvolvendo no centro de medicina regenerativa wake forest para transplantar em homens em breve. Vocês conseguem fazer uma coisa desse nível?
A ideia é essa Rodrigo, mas acho que ainda vamos precisar de alguns anos ou até décadas para conseguir criar um órgão vivo inteiro em laboratório, que possa ser transplantado.
Dr. Alessandro Zorzi, bom dia!
Tenho problemas com o meu ombro ( Manguito rotador) rompimento parcial dos tendões, gostaria de saber com a medicina regenerativa consigo resolver esse problema e onde posso encontrar esse profissional especializado nessa técnica para fazer esse procedimento com células troco e ácido hialurônico?
sergio, no momento o uso de celular tronco e de plaquetas não é autorizado no Brasil pelo CFM. Somente como pesquisa. O acido hialurônico pode ser usado e praticamente todos os ortopedistas podem te oferecer o tratamento.
Boa noite, minha bebê tem plaquetas baixas devido a gene Rap 1 b vcs tem um tratamento para esse gene ou estudo ?