Síntese de RNA em água, sem polimerase
Quão longe estamos de compreender como surgiu a vida no planeta Terra? Fica difícil de imaginar, se levarmos em conta todos os esforços realizados ao longo dos últimos quase 60 anos, desde que Miller publicou o primeiro trabalho simulando reações da atmosfera terrestre primitiva antes do surgimento da vida. Desde então, o volume de pesquisas realizado neste ramo do conhecimento, chamado de “química pré-biótica” (química de antes da vida), só têm aumentado. Os trabalhos mais recentes apresentam resultados incríveis, e demonstram que talvez estejamos muito próximos de conseguir simular o surgimento de um “sistema vivo” em laboratório.
O grupo de pesquisas coordenado por Ernesto Di Mauro, da Universitá La Sapienza di Roma, publicou recentemente artigo na prestigiosa revista Journal of Biological Chemistry, que relata a síntese de longas cadeias de RNA (ácido ribonucléico) em água. Porque este trabalho é importante? Por vários motivos.
Em primeiro lugar, porque a reação química de “união” de monômeros do RNA, os assim chamados nucleotídeos (monofosfatos de citidina, guanosina, adenosina e uridina), é uma reação de condensação que tem a eliminação de uma molécula de água como produto secundário. Este é um fator complicador para que esta reação ocorra em meio aquoso, pois se produz água não deveria acontecer, uma vez que o ambiente já está cheio de água. Sendo assim, dentro das células esta reação requer o uso de enzimas, chamadas de RNA polimerases, que “ajudam” esta reação a acontecer.

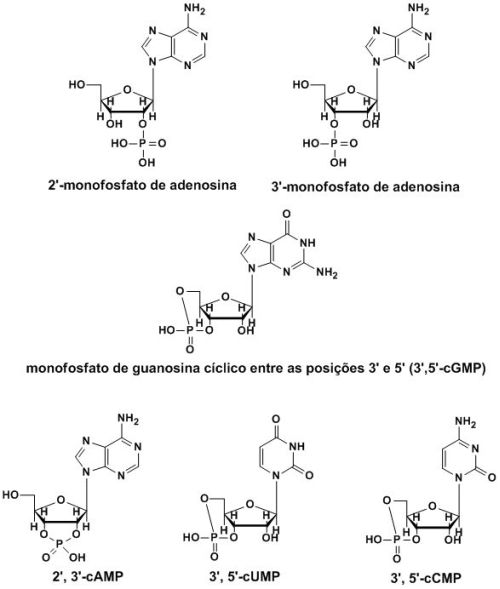
O grupo de Di Mauro utilizou nucleotídeos de RNA ligeiramente diferentes daqueles utilizados nas células. Os das células apresentam seu grupo fosfato “livre”, ou seja, pronto para se unir a outra unidade de nucleotídeo. Os pesquisadores italianos utilizaram nucleotídeos nos quais o grupo fosfato está ligado internamente a dois grupos OH, e por isso se encontra ciclizado. Desta maneira, o monômero ciclizado apresenta uma “maior energia”, pois, quando reage o grupo fosfato “se abre”, e libera energia para o meio em que se encontra. A quantidade de energia liberada compensa o fato de a reação estar sendo realizada em água. Por isso, a reação ocorre. É uma idéia simples, e que foi utilizada de maneira muito inteligente pelos autores. Para que esta reação ocorra sem a necessidade de um catalisador (que acelera a reação diminuindo a energia livre de ativação; no caso a RNA polimerase), tal processo deve se basear em compostos que são intrinsecamente reativos, estáveis (que não se decomponham), de natureza química simples e que forneçam um produto similar àquele esperado (ou seja, polinucleotídeos).
Os autores inicialmente testaram a reação entre unidades de 2′-AMP (monofosfato de 2′-adenosina) ou entre unidades de 3′-AMP (mas não entre as duas), a temperaturas entre 40º e 90º C, durante 400 horas, sem sucesso. Todavia, quando utilizaram 3′,5′-cGMP (monofosfato de guanosina cíclico entre as posições 3′ e 5′), observaram o surgimento de cadeias com até 25 monômeros interligados. A reação foi realizada a 85º C, em uma concentração de 1 mM (0,001 moles/litro). Acima desta concentração a reação termina após a formação de uma cadeia com 8 unidades de nucleotídeos. Os autores observaram que o processo de formação da cadeia ocorre um duas etapas. Primeiro se formam pequenas cadeias, as quais depois passam a se unir, formando uma “população” de cadeias de diferentes tamanhos. A reação continuou durante 200 horas, quando os autores observaram cadeias com mais de 100 unidades de monômeros ligados entre si. Fato interessante, a reação entre unidades de 2′,3′-cAMP levou somente à formação de pequenas cadeias. Já a reação entre 3′,5′-cUMP e entre unidades de 3′,5′-cCMP forneceu apenas cadeias muito pequenas.
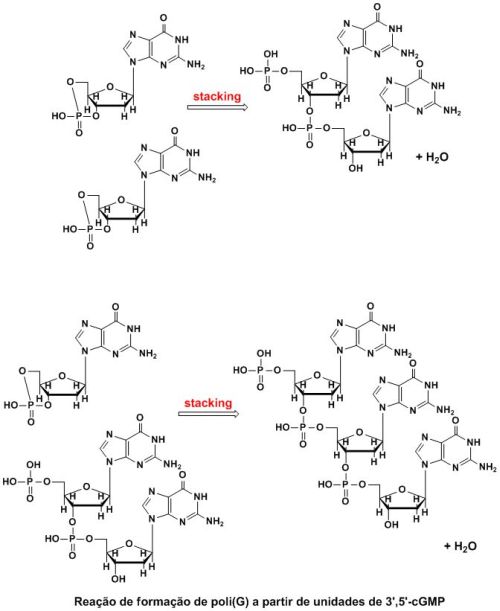
Como ocorre a reação? Bem, os autores propõem que esta ocorre através de um processo denominado “stacking”, durante o qual a ligação 3′,5′-fosfato de um nucleotídeo se abre e reage imediatamente com o oxigênio da posição 3′ de outro nucleotídeo. Assim, o grupo fosfato “pendurado” na posição 5′ vai reagindo seguidamente com o oxigênio da posição 3′ de outros nucleotídeos, e a cadeia de RNA vai aumentando de tamanho.
De maneira a estabilizar a cadeia, denominada de poli(G) (monofosfato de guanosina polimerizado), os autores adicionaram o polímero complementar, poli(C) (monofosfato de citidina polimerizado). Como se sabe, no interior das células, os nucleotídeos se estabilizam formando pares, através de ligações hidrogênio. A citidina forma par com guanosina, e a adenosina forma par com a timidina, no DNA. Desta maneira, duas cadeias se estabilizam e formam cadeias complementares, pareadas. Estas dão origem à chamada “dupla hélice” que constitui o DNA (ácido desoxirribonucléico). Ao adicionar poli(C) os autores promoveram a estabilização adicional da cadeia de poli(G) sintetizada.
Após a síntese, os pesquisadores investigaram o tempo de meia vida dos polímeros formados (o tempo de meia vida é o tempo necessário para que a quantidade dos polímeros formados diminua até a metade da quantidade formada inicialmente), e observaram que o tempo de meia vida dos polímeros formados a partir de 3′,5′-cGMP e de 3′,5′-cAMP são excepcionalmente longos. Ou seja, são polímeros estáveis, que duram muitas horas. E por isso podem, em princípio, exercer funções bioquímicas.
A grande questão é: bom, OK, os autores utilizaram monômeros do tipo 3′,5′-cXMP (onde X pode ser G, guanosina; A, adenosina; C, citosina; ou U, uridina) para realizar a reação de polimerização “espontânea” em água. Mas, será que estes monômeros podem ocorrer naturalmente com o grupo fosfato ciclizado? Sim. Trabalhos anteriores (citados no trabalho publicado) relataram a formação destes nucleotídeos, seja na presença de fosfato livre ou na presença de minerais de fosfato.
O interessante das reações realizadas é que estas não necessitam pré-ativação dos nucleotídeos, não necessitam de catalisador, e a polimerização ocorre em meio aquoso. A reação de polimerização ocorre através do processo de um processo denominado “stacking”, que é um tipo de “interação explosiva” entre os nucleotídeos, que resulta na rápida reação entre estes, formando a ligação éster de fosfato entre dois monômeros. O processo de “stacking” depende diretamente do pH do meio onde a reação ocorre, bem como da temperatura e do tamanho das moléculas que reagem. Em geral, reações através de “stacking” são favorecidas em baixas temperaturas, baixos pHs e moléculas longas.
O trabalho desenvolvido pelo grupo de Di Mauro é mais um exemplo de que a formação de oligômeros (pequenos polímeros) e polímeros de nucleotídeos (unidades monoméricas que dão origem ao RNA ou ao DNA) é possível de ocorrer em condições muito simples. Tais condições refletem, de certa maneira, o ambiente terrestre primitivo, no qual os precursores do RNA e do DNA que conhecemos devem ter surgido. Como ilustrado em outro artigo, publicado no início deste ano na revista Science, tais protótipos de RNA são passíveis de sofrer seleção natural. Assim, os mais estáveis serão selecionados, e se perpetuarão através de processos de duplicação. Resta saber como estes polímeros se transformaram em moléculas transportadoras de informação. Mas isso é outra história.
O artigo completo de G. Constanzo, S. Pino, F. Ciciriello e E. Di Mauro, “Generation of Long RNA Chains in Water”, The Journal of Biological Chemistry, 2009, vol. 284, 33206-33216, pode ser baixado aqui, para aqueles que têm acesso à assinatura da revista.
Quando a verdade dói
Nada mais incômodo sabermos de algo que nos incomoda profundamente. Uma crítica bem feita, ainda que de maneira agressiva, mas que no fundo é verdade, dói. Tomarmos consciência de nossas limitações, sejam estas quais forem, costuma doer. Receber uma má notícia de um médico competente, dói muito. Muito mesmo. A verdade muitas vezes dói. Mas é uma dor que nos leva a crescer e amadurecer. Profissionalmente, ou em termos pessoais. Reconhecer a dor da verdade e aceitar os fatos constitui um dos processos mais importantes para nossa formação.
Porém, muitas vezes preferimos esconder, e fazer de conta que a verdade não está presente.
Fatos recentes ilustram como aceitar a verdade dos fatos pode ser difícil. O apagão do dia 11/11/2009 ilustra bem este caso. Logo após o evento, o ministro de Minas e Energia, Edison Lobão, manifestou-se dizendo que a causa seriam raios perto da região de Itabera. Argumento confirmado pela ministra chefe da Casa Civil, Dilma Roussef. Todavia, pouco tempo depois engenheiros do Instituto Nacional de Pesquisas Espaciais (INPE) afirmaram que
“Embora houvesse uma tempestade na região próxima a Itabera, no sul de São Paulo, com atividade de descargas no horário do apagão, as descargas mais próximas do sistema elétrico estavam a cerca de 30 km da subestação de Itabera e a cerca de 10 km de uma das quatro linhas de Furnas de 750 kV e cerca de 2 km de uma das outra linhas de 600 kV, que saem de Itaipu em direção a São Paulo. Além disso, a baixa intensidade da descarga registrada [menor que 20 kA] não seria capaz de produzir um desligamento da linha, mesmo que incidisse diretamente sobre ela, como também confirma a Rede Brasileira de Detecção de Descargas, que estava no momento do apagão operando com ótimo desempenho. Em geral, apenas descargas com intensidade superiores a 100 kA, atingindo diretamente uma linha, podem causar um desligamento de linhas de transmissão operando com tensões tão elevadas como as linhas de Itaipu [duas de 600 kV e duas de 750 kV].”
As declarações do INPE causaram profundo desconforto no governo. No dia seguinte o ministro das Minas e Energia desqualificou as declarações do INPE que, no entanto, deu suporte às declarações do engenheiro apresentadas no Jornal Nacional. Afinal, quem falou a verdade? Embora as reais causas do apagão ainda não tenham sido estabelecidas, ficou evidente que o governo não gostou do ocorrido, e tentou minimizar o fato. Porém, o importante não é esconder o problema, e sim conhecê-lo. Como disse o técnico do INPE, se o sistema de distribuição de energia elétrica fosse suscetível a raios de tão pequena intensidade, sua fragilidade estaria atestada. No mesmo dia o presidente Lula declarou que seria necessário se investigar a real causa do problema. As declarações apressadas para justificar o injustificável apenas pioraram o quadro geral que se formou depois do blecaute. Melhor é esperar para se conhecer as reais causas do ocorrido, para que estas possam ser posteriormente evitadas.
Anterior ao blecaute brasileiro foram as declarações de David Nutt, professor do Imperial College London e [ex-]presidente do comitê assessor do governo britânico sobre abuso de drogas, que causaram polêmica: o consumo de álcool e tabaco seria pior para a saúde do que o consumo de maconha, LSD e ecstasy. Nutt foi recentemente demitido de suas funções, fato que gerou protestos veementes da comunidade científica inglesa, que considera o ato do governo como sendo de extrema arbitrariedade. O governo inglês questionou a capacidade científica e profissional de Nutt. Porém, o que Nutt ganhou apresentando os fatos sobre o uso de drogas? E o que será que o governo inglês perderia caso aceitasse os fatos apresentados por Nutt?
É, muitas vezes a verdade dói.





