O Prêmio Nobel de química de 2017 foi concedido aos pesquisadores que estão na vanguarda da inovação no campo da visualização tridimesional de biomoléculas. De acordo com a citação do prêmio, Jacques Dubochet (Universidade de Lausanne), Joachim Frank (Universidade de Columbia) e Richard Henderson (MRC Laboratory of Molecular Biology em Cambridge, Reino Unido) merecem o prêmio pelo desenvolvimento de um método de “Crio-Microscopia Eletrônica para a determinação da estrutura de alta resolução de biomoléculas em solução”.
O que isso significa em termos mais simples?
Com o uso dessa técnica revolucionária de crio-microscopia eletrônica os pesquisadores conseguiram “congelar” as biomoléculas. E, dessa forma foi possível visualizar as estrutura tridimensional das biomoléculas com alta qualidade. Em outros termos, eles conseguiram visualizar as moléculas biológicas tridimensionais ainda mais perto olhando átomo por átomo.
Qual a importância dessa visualização tridimensional de biomoléculas?
Uma imagem é uma chave para a compreensão. Os avanços científicos geralmente se baseiam na visualização bem-sucedida de objetos invisíveis ao olho humano. No entanto, os mapas bioquímicos foram preenchidos com espaços em branco porque a tecnologia disponível até aquele momento ainda tinha dificuldade em gerar imagens de grande parte da maquinaria molecular da vida.
Os microscópios crio-electrônicos mudam tudo isso. Os pesquisadores agora podem congelar as biomoléculas no meio do movimento biológico e visualizar os processos celulares que nunca antes tinham visto. A visualização de imagem detalhada de biomoléculas é decisivo para a compreensão dos processos biológicos.
No post anterior, Fármacos e Química – Interações na sua vida, nós vimos que os alvos moleculares como enzimas, canais iônicos, moléculas transportadoras e ácidos nucléicos são aparatos essenciais na maquinaria celular. Dessa forma, enxergá-los com alta resolução é essencial para o desenvolvimento de farmacos, por exemplo.
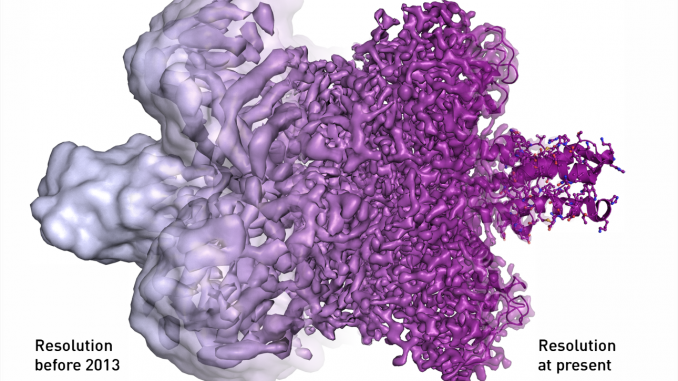
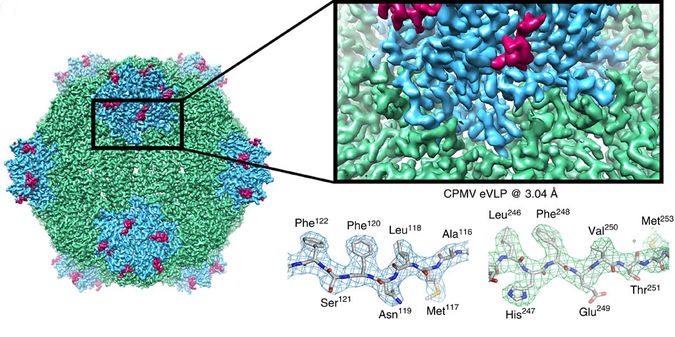
O microscópio crio-eletrônico permitiu que os cientistas explorassem a arquitetura de uma variedade de biomoleculas, desde as proteínas que causam resistência aos antibióticos à superfície do vírus Zika. No ano passado, a estrutura 3D da enzima que produz o amilóide da doença de Alzheimer foi publicada usando esta tecnologia. Na Figura 1, temos uma imagem que demonstra o uso da microscopia de crio-elétron na reconstrução de uma parte de vírus que antes estava inacessível com a tecnologia antiga.
No futuro próximo, a compreensão das configurações e estabilidade das biomoléculas em temperaturas ultra baixas também pode acelerar os esforços de criobiologia, onde os cientistas estão focados em como vitrificar os tecidos e órgãos humanos para que possam ser preservados por longas durações.
Alimente seu cérebro com QuimiKinha!
CIÊNCIA PARA TODOS!
Referências bibliográficas
[1] Press Release: The Nobel Prize in Chemistry 2017
[2] Hesketh EL, Meshcheriakova Y, Dent KC, et al. Mechanisms of assembly and genome packaging in an RNA virus revealed by high-resolution cryo-EM. Available from: https://www.nature.com/articles/ncomms10113


Faça um comentário