Texto por Mellanie Fontes-Dutra, Lívia Okuda Santos e Ana de Medeiros Arnt
Coronavírus: é uma família de vírus? De onde vêm? A quem infecta? Tem vírus novo? Os morcegos têm culpa no cartório? Pois bem, hoje vamos responder estas e mais algumas dúvidas no texto do Especial de hoje.
O que é Coronavírus?
O Coronavírus é uma família de diferentes vírus existentes na natureza. Alguns infectam humanos e outros não. Assim, nesta família viral, existem alguns vírus que causam resfriados e outros que podem causar síndromes respiratórias graves, como COVID-19. Mas temos um novo integrante, recém descoberto, nessa grande família e vamos falar mais dele neste texto!
Olhando para nossa história, já tivemos pandemias ou risco de pandemias com os coronavírus: pelo SARS-CoV-1 (2002), MERS-CoV (2012) e SARS-CoV-2 (2019). Aliás, as pandemias, como sabemos agora, são eventos causados por patógenos (como vírus ou bactérias) que atingem o mundo inteiro, causando preocupação e danos à saúde da população de muitos países.
Pode parecer novidade para muitas pessoas, mas existe monitoramento epidemiológico no mundo inteiro de possíveis patógenos pandêmicos, incluindo os diversos coronavírus que encontramos em espécies selvagens ou domésticas. Isto nos ajuda a saber se são ou estão se tornando perigosos para os humanos.
Então, depois desse background, podemos falar sobre o nosso tema de hoje: Sars e os Neo-Cov. Sendo o primeiro o grupo do nosso conhecido e odiado COVID-19, e o segundo um tipo de coronavírus encontrado recentemente na África.
Origem do SARS-COV-2: hipótese zoonótica.
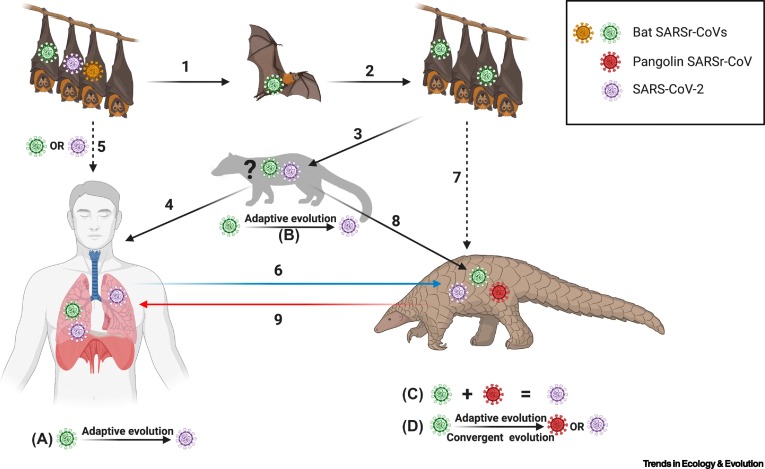
Análises filogenéticas recentes identificaram que os SARS-CoVs provavelmente divergiram de um coronavírus ancestral derivado de morcego entre 1948 e 1982. Filogenia é a área da biologia que estuda a “ancestralidade” dos vírus e seres vivos, a partir de análises genéticas e moleculares, traçando assim sua “história evolutiva”.
Este estudo sugere que os vírus tipo os SARS-CoVs têm circulado em espécies selecionadas de morcegos há algum tempo. Existem trabalhos que mostraram uma grande semelhança de coronavírus que infectam morcegos com o SARS-CoV-2, apresentando até 96,1% semelhança no material genético, como no caso do estudo recente em Laos.
Assim, é possível que a linhagem originária do SARS-CoV-2 tenha circulado despercebida em morcegos por décadas.
Em outro estudo constatou-se a ocorrência de uma frequente troca de coronavírus entre morcegos. Aliás, é sempre bom lembrar que eles são animais que podem viver aglomerados, podendo gerar uma grande diversidade genética e novas versões de vírus.
Também é possível que um SARS-CoV tenha evoluído para SARS-CoV-2 em humanos após o chamado spillover de um animal (transbordamento, ou quando um vírus de uma espécie passa a infectar outra espécie diferente) seguido pela rápida transmissão desta cepa (tipo de vírus) adaptada a humanos. Portanto, é um desafio para a comunidade científica estimar a frequência do transbordamento zoonótico.
Vamos entender melhor como uma pesquisa assim pode ser feita?
Pesquisadores, em um estudo ainda em preprint, criaram um mapa detalhado de habitats de 23 espécies de morcegos conhecidas por abrigar coronavírus relacionados ao SARS. Nesta pesquisa, sobrepuseram dados sobre onde os humanos vivem para criar um mapa de potenciais pontos de infecção. Visto isso, cerca de 500 milhões de pessoas vivem em áreas onde podem ocorrer spillovers, incluindo o norte da Índia, Nepal, Mianmar e boa parte do Sudeste Asiático. Logo, esta informação pode nos dar pistas de locais em que essa vigilância precisa ser frequente e fortificada.
Interessante, não? Uma pesquisa que vai não só analisar habitats de animais infectados, mas relacionar-se às populações humanas que podem ter contato frequente com estes animais. Este é um dos modos de realizarmos monitoramentos e termos dados mais precisos (e constantes) de riscos para nós.
Quer dizer que o vírus não foi feito pelos laboratórios chineses comunistas?
É isso mesmo, ao que tudo indica a origem do SARS-CoV-2 é natural, de morcegos ou outros animais.
Essa afirmação pode ser compreendida melhor com o artigo que relata um vírus muito relacionado ao SARS-CoV-2 já circulava desde 2010 em Camboja. Este artigo adiciona mais uma evidência da origem natural desse vírus. Além disso, mais recentemente, foi descoberto que no norte do Laos alguns vírus muito parecido com o SARS-CoV-2 circulam em morcegos, os quais apresentam particularidades que os relacionam muito proximamente ao vírus da COVID-19.
E esse spillover não dá em nada?
Segundo o preprint já citado, e tendo cuidado com as limitações do dado obtido, cerca de 400.000 pessoas estão provavelmente infectadas com coronavírus relacionados à SARS todos os anos, em transbordamentos que nunca se transformam em surtos detectáveis.
“Mas por que, se temos todas essas infecções anualmente, não vemos muitos surtos?”
Porque a maioria das infecções ocultas têm vida curta e não levam à transmissão, em razão de os vírus não serem bem adaptados aos humanos. Em geral, alguns humanos podem se infectar diretamente do contato com animais, mas acabam não transmitindo a outros seres humanos, acabando ali mesmo com a infecção. O problema é se a frequência delas se tornar alta, o que pode propiciar a transmissão entre seres humanos.
Ainda, existe outro risco! Muitas dessas infecções, exatamente por serem “novas”, podem gerar diagnósticos errados, exatamente por sintomas que se assemelham a outras doenças. No caso da COVID-19, por exemplo, os primeiros diagnósticos saíam como gripe ou pneumonia, até que se percebesse que existia um novo patógeno infectando ali! Isto também adiciona um viés ao dado. Soma-se a isso toda uma discussão sobre o acesso à saúde que pessoas de regiões rurais possuem, e isso é uma questão importante.
Só morcego pode passar doença para humano?
Na verdade não. Em geral, o monitoramento de vírus que podem fazer o spillover aponta que existem vários vírus – de Influenza por exemplo – que indicam outros animais, especialmente aves. A gente já ouviu falar da gripe aviária e gripe suína, que são vírus da família Influenza. Portanto, tanto espécies ditas como “domésticas”, quanto espécies que vivem em ambientes selvagens podem estar envolvidas em spillover.
Mas em se tratando de coronavírus, apesar de os morcegos serem fortíssimos candidatos a reservatórios desta família, não podemos afirmar com certeza se existem ou não outros animais possíveis. No caso do surto de SARS-CoV em 2002, as Civetas foram um provável candidato, por exemplo.
E aquele bichinho da China, o pan… pe… pebolim?
Ah, quer dizer o Pangolin? SIM! Existe a possibilidade de o pangolin ter entrado de bobo nessa história. Ou seja, ser um hospedeiro intermediário entre o possível reservatório do vírus (morcego) e nós. Mas ainda precisamos de mais análises para entender se sim, e como isso ocorreu.
Essa situação não seria algo improvável, já que algumas famílias de morcegos (como o Rhinolophidae) compartilham algumas dietas com os pangolins na natureza. E por fim, temos fatores ecológicos que propiciaram esses spillovers. Urbanização, deflorestamento, redução de habitats selvagens forçam uma proximidade dessas espécies conosco, favorecendo contatos e exposições.
Entretanto, analisando os SARS-CoVs, nota-se uma semelhança de mais ou menos 85,5 -92,4% ao SARS-CoV-2 em seu material genético. Além disso, possuem semelhanças intrigantes com o vírus em regiões que são fundamentais para a interação com nossas células. Especificamente, existe uma região do vírus, conhecida como RBD (sigla para receptor-binding domain), que é exatamente onde o vírus se liga com o ACE2 de nossas células, para entrar nelas. Esta região de um SARS-CoV de pangolim tem 97,4% de semelhança com o do SARS-CoV-2, o que é muito intrigante e mostra que existe muito ainda para conhecermos e, também, que a identificação filogenética destes vírus não é tão simples, tendo em vista que pode haver troca de materiais virais em animais hospedeiros. Isto é, os diferentes tipos de coronavírus que infectam um animal, podem trocar materiais genômicos (que conhecemos como recombinações).
Mas o Mercado de Huanan tem alguma coisa a ver?
Vamos falar disso agora! Vimos anteriormente que os morcegos eram o reservatório do ancestral do SARS-CoV-2, certo? Também sabemos que este mercado é conhecido por ter bancas que vendem animais vivos, como o cão-guaxinim, que já foi associado a emergência do SARS-CoV-1 e que é não só suscetível ao SARS-CoV-2, como capaz de transmiti-lo.
Aliás, por meio de análises espaciais, um artigo demonstrou que os primeiros casos relatados de COVID-19 em dezembro de 2019 foram distribuídos geograficamente próximos e centrados no mercado de Huanan, em Wuhan. Assim, os autores comentam que essa proximidade de casos ao mercado de Huanan foi, em Dezembro de 2019, maior que o esperado, dada a densidade populacional de Wuhan ou a distribuição espacial dos casos de COVID mais tarde na epidemia, sugerindo o epicentro no mercado.
Todavia, o mais interessante é que, considerando o próprio mercado, os dados desse trabalho sugerem que um grande número de casos estava ligado ao setor oeste do mercado, onde a maioria das bancas que vendiam animais vivos se concentravam. Somando os dados, é plausível que várias espécies de mamíferos suscetíveis ao SARS-CoV-2 e que poderiam ser hospedeiros intermediários de seus “parentes ancestrais” foram vendidos vivos no mercado de Huanan em novembro de 2019 e podem ter contribuído para a transmissão.
Pois é! Há indícios de que não foi “uma só infecção”!
Deste modo, é provável que houvesse vários animais infectados no mercado de Huanan e pode ter havido pelo menos duas “entradas” do SARS-CoV-2 (linhagens A e B) em humanos, com a entrada da linhagem B e algumas semanas após, a linhagem A.
A linhagem A do vírus, a qual não havia sido encontrada no mercado de Huanan, tem uma associação geográfica imensa com esse mercado, sugerindo que “as linhagens A e B surgiram nesse mercado e começaram a se espalhar para a comunidade residencial de Wuhan”. Dessa forma, os autores dizem que
“Amostras positivas para SARS-CoV-2 estavam fortemente associadas à venda de mamíferos vivos, particularmente no canto sudoeste do mercado de Huanan, onde amostras ambientais positivas provavelmente foram derivadas de animais infectados”
Outro artigo concluiu que a circulação de um vírus ancestral em morcegos, que passou a ser capaz de ligar em ACE2, “pulou” para hospedeiros intermediários (animais suscetíveis) que foram comercializados vivos no mercado de Huanan, surgindo as linhagens A e B pouco tempo depois e a infecção em humanos.
A importância de monitoramentos ambientais e pesquisa básica!
Sim, voltaremos a este tema, pois além de informações interessantes e fundamentais para compreendermos melhor o mundo que vivemos, também usamos estas informações para entender a importância da pesquisa científica! Recentemente, o vírus Neo-CoV foi encontrado entre morcegos na África do Sul. Cientistas chineses alertaram para esse vírus, no entanto, falta ainda um entendimento maior sobre seu potencial infeccioso.
Neo-Cov: quem é e o que sabemos dele?
Primeiro, um spoiler: não é uma nova variante do vírus da COVID-19, e não é algo novo no geral!
O Neo-CoV é um outro tipo de coronavírus que foi relatado pela primeira vez em 2012 e em 2015 durante o surto de MERS-CoV que pode usar receptores ACE2 de morcegos, mas não os receptores ACE2 de humanos. E, até o presente momento, não se observou infecção em humanos em sua forma atual, espalhando-se exclusivamente entre os morcegos.
De acordo com especialistas, as descobertas feitas pelos cientistas de Wuhan não representam um risco para a humanidade no momento atual. Apenas apontam para a necessidade de se acompanhar mais um tipo de coronavírus e sua evolução.
O Neo-CoV ganhou a atenção da mídia pelo fato de os cientistas chineses disponibilizarem esses dados recentes (e importantes) em um preprint. Assim, este vírus é na verdade um vírus intimamente relacionado ao MERS-CoV que entra nas células através dos receptores DPP4 e pode usar o ACE2
Finalizando
Por fim, imagino que não seja possível negar a importância do monitoramento epidemiológico e do investimento nesta ciência, não é? É muito provável que, para praticamente qualquer patógeno zoonótico da vida selvagem, o transbordamento é mais frequente do que anteriormente reconhecido. E precisamos de mais investimento em ciência e vigilância genômica para monitorá-los de maneira pública para que possamos controlar epidemias e evitar que novas pandemias, como COVID-19, apareçam.
Além disso, também é sempre bom lembrar que não é culpa dos animais estas infecções. Portanto, não deveríamos interferir ainda mais nos habitats deles e causar danos e diminuição das populações silvestres. Os monitoramentos devem ser no sentido de compreendermos quais são os vírus presentes nestes animais e, também, estabelecermos formas de preservação e diminuição de interações que sejam prejudiciais para nós, enquanto espécie, e para estas espécies silvestres.
Parte das infecções ocorre (e pode ocorrer) especialmente pela invasão de habitats destes animais, aumentando o contato entre seres humanos e espécies de ambientes naturais.
Para saber mais:
LAM, Tommy Tsan-Yuk; JIA, Na; ZHANG, Ya-Wei; et al (2020) Identifying SARS-CoV-2-related coronaviruses in Malayan pangolins Nature, v 583, n 7815, p 282–285, 2020.
XIAO, Kangpeng; ZHAI, Junqiong; FENG, Yaoyu; et al (2020) Isolation of SARS-CoV-2-related coronavirus from Malayan pangolins Nature, v583, n7815, p 286–289.
ZHANG, Yong-Zhen ; HOLMES, Edward C (2020) A Genomic Perspective on the Origin and Emergence of SARS-CoV-2 Cell, v 181, n 2, p 223–227.
BONI, Maciej F.; LEMEY, Philippe; JIANG, Xiaowei; et al (2020) Evolutionary origins of the SARS-CoV-2 sarbecovirus lineage responsible for the COVID-19 pandemic Nature Microbiology, v5, n11, p 1408–1417.
BANERJEE, Arinjay; DOXEY, Andrew C.; MOSSMAN, Karen; et al (2021) Unraveling the Zoonotic Origin and Transmission of SARS-CoV-2 Trends in Ecology & Evolution, v 36, n 3, p 180–184.
KUPFERSCHMIDT, SARS-like viruses may jump from animals to people hundreds of thousands of times a year. Science.org.
SÁNCHEZ, Cecilia A; LI, Hongying; PHELPS, Kendra L; et al (2021) A strategy to assess spillover risk of bat SARS-related coronaviruses in Southeast Asia.
FORATO, Fidel (2021) NeoCoV: tipo diferente de coronavírus chama atenção, mas não chegou em humanos Canaltech.
KUMAR, Ajeet (2021) NeoCov: What is WHO saying about newly discovered coronavirus found in bats? Republic World.
WOROBEY, Michael; LEVY, Joshua I; MALPICA, Lorena M; et al (2022) The Huanan market was the epicenter of SARS-CoV-2 emergence, Zenodo, 2022.
PEKAR, Jonathan E; MAGEE, Andrew; PARKER, Edyth; et al (2022) SARS-CoV-2 emergence very likely resulted from at least two zoonotic events Zenodo, 2022.
Observação 1:
Este texto foi organizado com informações complementares às publicações de Mellanie Fontes-Dutra
- E se eventos zoonóticos como o que provavelmente gerou o SARS-CoV-2 estiverem acontecendo centenas de milhares de vezes por ano?
- Sobre o Neo-CoV
- Origem do SARS-CoV-2
Observação 2
Há trechos desta postagem que são traduções livres de artigos, com adequações de linguagem para melhor compreensão do tema.
As Autoras
Ana Arnt é licenciada em biologia, doutora em educação, professora do Instituto de Biologia da Unicamp, coordena os projetos Blogs de Ciência da Unicamp e o Especial COVID-19.
Livia Okuda é estudante de Farmácia na Unicamp e divulgadora científica do Especial Covid-19 do Blogs Unicamp.
Mellanie Fontes-Dutra é biomédica, doutora em neurociência e pesquisadora na Universidade Federal do Rio Grande do Sul e Divulgadora Científica na Rede Análise COVID-19. Autora convidada no Especial COVID-19 e parte do projeto Todos Pelas Vacinas.
Este texto foi escrito originalmente para o Especial COVID-19.

Os argumentos expressos nos posts deste especial são dos pesquisadores. Dessa forma, produziu-se textos produzidos a partir de campos de pesquisa científica e atuação profissional dos pesquisadores. Além disso, a revisão por pares aconteceu por pesquisadores da mesma área técnica-científica da Unicamp. Assim, não, necessariamente, representam a visão da Unicamp e essas opiniões não substituem conselhos médicos.



0 comentário