Texto escrito por Fellipe Mello, Carla Maneira da Silva e Ana Arnt
No primeiro texto, falamos um pouco do desenvolvimento do teste diagnóstico para Covid-19 baseado em uma levedura modificada geneticamente. Mas agora, neste segundo texto, vamos explicar um pouco mais sobre o que são estas modificações e de que modo ela acontece na levedura. Isto é, vamos entrar um pouco mais a fundo no mundo da Engenharia Genética para entender melhor como a ciência trabalha e é produzida!
Levedura modificada geneticamente – o que estamos modificando nela?

Organismos geneticamente modificados (OGM) são mais comuns do que imaginamos. O ser humano tem utilizado vastamente o melhoramento genético em benefício da nossa sociedade. Por exemplo, a seleção de características de interesse em animais e plantas – que é traço de nossa organização social desde os primórdios. Além disso, temos a produção de químicos específicos por microrganismos,
O CORONAYEAST não é diferente: é um biossensor viral baseado em uma levedura que precisa ter seu genoma editado para servir a esse propósito. Para tal, precisamos inserir no microorganismo alguns genes heterólogos. Calma, o nome é difícil, mas a explicação é simples… Isto é, o que quisemos dizer é que são genes que a espécie Saccharomyces cerevisiae não possui naturalmente.
Como já falamos sobre o funcionamento do CORONAYEAST, podemos dividir essas modificações genéticas em três grupos principais: 1) proteína ACE2 de humano, responsável tanto pela percepção do SARS-CoV-2 quanto pelo controle do hormônio angiotensina II (já vamos explicar!); 2) receptor AT1 de humano, receptor de membrana da classe das proteínas do tipo G que consegue detectar angiotensina II e enviar um sinal pra célula; 3) os genes repórter, que produzem proteínas que conferem a mudança de cor e fluorescência na levedura e que são ativados pelo receptor AT1.
Agora é que vem a parte complicada e cheia de termos. Mas respira fundo aí que a gente vai explicar com calma um por um!
ACE2, AT1 e SARS-CoV-2: quê?
A ACE2 – Enzima Conversora de Angiotensina 2 é encontrada naturalmente em humanos. Assim, ela tem o papel de regular os níveis de Angiotensina II no nosso organismo, convertendo-a em Angiotensina 1-7.
A Angiotensina II é um hormônio peptídeo que atua na vasoconstrição e, junto com a ACE2, faz parte do sistema renina-angiotensina (RAS), que é um intricado e complexo sistema de regulação da nossa pressão arterial. Além disso, também estão presentes os receptores de membrana, como o AT1. O AT1, como dissemos, consegue perceber a concentração de angiontesina II no meio e enviar um sinal para a célula reagir em conformidade. Ou seja, a resposta celular varia de acordo com a quantidade do hormônio detectado. Ademais, esse receptor de membrana faz parte da classe dos GPCR. Ou seja: o AT1 reage apenas à presença de angiotensina II e consegue detectar baixas concentrações deste hormônio.
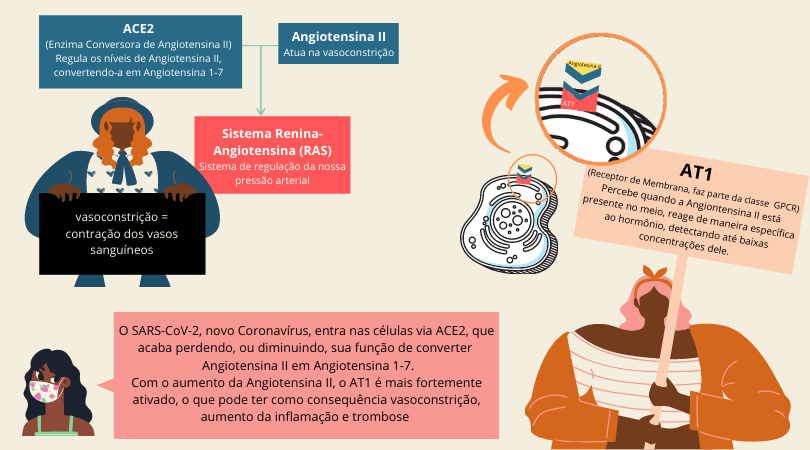
Todavia, o entendimento de todo esse sistema é importante não apenas para entender o CORONAYEAST. Foi essencial também para elucidar os efeitos da COVID-19 em pacientes. O SARS-CoV-2 tem apenas uma forma de infectar nossas células: através da ligação com a ACE2 . Portanto, ao detectar uma possível célula hospedeira, o SARS-CoV-2 se liga a essa enzima e faz com ela não consiga desempenhar seu papel normalmente. Resumindo: quando o vírus nos infecta, o ACE2 fica comprometido e, por isso, apresentamos maiores níveis de angiotensina II.
Mas e o gene repórter? Pois é, Faltou explicar este último dos 3 elementos que precisamos modificar na levedura: o ACE2, o AT1 e o Gene Repórter…
Gene Repórter: o que é e por que ele é necessário?
Para fechar o sistema biossensor, precisamos de um, ou mais, gene repórter. Entretanto, para ficar claro o porquê e como vamos usar esse artefato, precisamos de uns conceitos básicos de genética. Mas calma, não é nada muito complicado. O que precisamos saber é que os genes são estruturas formadas de subunidades que regulam sua expressão. Ou seja: pra um gene ativar e produzir uma proteína ele precisa estar sob uma condição específica. Por fim, quem regula essa condição e diz se o gene deve ativar é o promotor. Isto é: não basta um ser vivo “ter um gene” para determinada função. Assim, este gene precisa de um agente externo (o promotor) para ser ativado (e produzir uma proteína que funcione!).
Mas, e o Gene Repórter? É um gene que é inserido junto com os genes de interesse da nossa pesquisa. Dessa forma, no nosso caso da Levedura Saccharomyces cerevisiae, o gene que produz o ACE2 e o gene que produz o AT1. Isto é, quando produzimos um Organismo Geneticamente Modificado, podemos também inserir um gene repórter junto com os genes que queremos que funcionem naquele organismo. Por quê? O gene repórter tem uma atividade facilmente rastreável – produz proteínas luminescentes ou que promovem mudança de cor, por exemplo. Em suma, com isto conseguimos saber que os genes que inserimos estão “funcionando”.
Assim, no caso desta levedura, o gene repórter produz proteínas que conferem a mudança de cor e fluorescência. Quer dizer, isso quando ativadas pela sinalização dentro da célula gerada pelo receptor AT1!
Para finalizar: o que tudo isto têm a ver com o teste CORONAYEAST?
Por fim, depois de explicar todos os genes, receptores, hormônios e enzimas que estão envolvidos na técnica, vamos voltar ao RAS? Lembra que o AT1 percebe a presença de angiotensina II e envia um sinal para a célula?
Pois bem, esse sinal diz pra um promotor específico, o FIG1, que ele deve ativar um gene. No caso do nosso biossensor, a gente vai colocar um gene repórter regulado pelo FIG1. Na verdade, vamos colocar dois (e por isso falamos que o CORONAYEAST pode ser usado no laboratório ou em casa). Quais? Um gene que produz uma proteína fluorescente e um gene que produz um pigmento visível à olho nu.
Mas, como isso tudo funciona na presença e ausência do vírus? Agora que explicamos tudo isso, no próximo texto vamos falar com mais detalhes sobre a interação da levedura com o vírus mais apropriadamente!
Este texto foi elaborado a partir de uma pesquisa financiada pela FAPESP, cujo processo é n.2018/03403-2
Força Tarefa da Unicamp
A pesquisa que embasou esta postagem é fruto da “Força Tarefa da Unicamp”. Assim, faz parte de um conjunto pesquisas científicas que a Unicamp vem fazendo desde o início da pandemia. O Especial Covid-19, do Blogs de Ciência da Unicamp, participa da Força Tarefa desde o início, com a divulgação científica sobre a doença. Mas também vai se dedicar à publicação destes conhecimentos produzidos especificamente pelos pesquisadores da Unicamp cada vez mais! Acompanhe as próximas postagens!
Nossos sites institucionais:
Para saber mais
Adeniran A, Sherer M, Tyo KEJ (2015) Yeast-based biosensors: Design and applications FEMS Yeast Res;15:1–15.
Azzi L, Carcano G, Gianfagna F et al (2020) Saliva is a reliable tool to detect SARS-CoV-2 J Infect 2020;81:e45–50.
Burrell LM, Johnston CI, Tikellis C et al. ACE2, a new regulator of the renin–angiotensin system. Trends Endocrinol Metab 2004;15:166–9.
Imai Y, Kuba K, Rao S et al (2005) Angiotensin-converting enzyme 2 protects from severe acute lung failure Nature 2005;436:112–6.
Nakamura Y, Ishii J, Kondo A (2014) Construction of a yeast-based signaling biosensor for human angiotensin II type 1 receptor via functional coupling between Asn295-mutated receptor and Gpa1/G i3 chimeric Gα. Biotechnol Bioeng;111:2220–8
Takata, R (2010) O que é um gene repórter afinal?Gene Repórter
Verdecchia, P, Cavallini, C, Spanevello, A, & Angeli, F (2020) The pivotal link between ACE2 deficiency and SARS-CoV-2 infection European journal of internal medicine, 76, 14–20.
Zhang H, Penninger JM, Li Y et al (2020) Angiotensin-converting enzyme 2 (ACE2) as a SARS-CoV-2 receptor: molecular mechanisms and potential therapeutic target Intensive Care Med 2020;46:586–90.
Os Autores
Ana Arnt é Bióloga, Mestre e Doutora em Educação. Professora do Departamento de Genética, Evolução, Microbiologia e Imunologia, do Instituto de Biologia (DGEMI/IB). Pesquisa e da aula sobre História, Filosofia e Educação em Ciências, e é uma voraz interessada em cultura, poesia, fotografia, música, ficção científica e… ciência!
Carla Maneira da Silva Mestranda em Genética de Micro-organismos pela Universidade Estadual de Campinas (UNICAMP). Realiza suas atividades de pesquisa no Laboratório de Genética e Bio-Energia (LGE). Possui experiência na área de genética e engenharia metabólica. Mais especificamente na produção de compostos de interesse econômico a partir de micro-organismos. Assim como na produção de biossensores baseados em levedura.
Fellipe Mello é Engenheiro químico (2014) e doutor em ciências (2019) pela Universidade Estadual de Campinas. Atualmente é post doc em engenharia genética no Laboratório de Genômica e bioEnergia no Instituto de Biologia da Unicamp. Tem experiência na área de engenharia química, com ênfase em termofluidodinâmica, no reaproveitamento de biomassas e purificação de proteínas; e na área de genética, com ênfase em engenharia metabólica e estudo de QTLs.
Este texto é original e escrito com exclusividade para o Especial Covid-19




0 comentário