Texto escrito por Fellipe Mello, Carla Maneira da Silva e Ana Arnt
Até esse ponto, nos textos anteriores, introduzimos uma variedade de conceitos importantes no desenvolvimento do conceito da CORONAYEAST. Vocês podem recapitular as ideias aqui e aqui.
Vamos revisar as modificações genéticas que a S. cerevisiae deve apresentar para detectar o vírus:
- O receptor do vírus e regulador da Angiotensina II (ACE2),
- O “detector” de angiotensina (AT1)
- As proteínas que fazem a levedura biossensora mudar de cor (os genes repórter).
Tá, e como isso tudo vai funcionar de forma que a levedura irá acusar a presença do vírus?
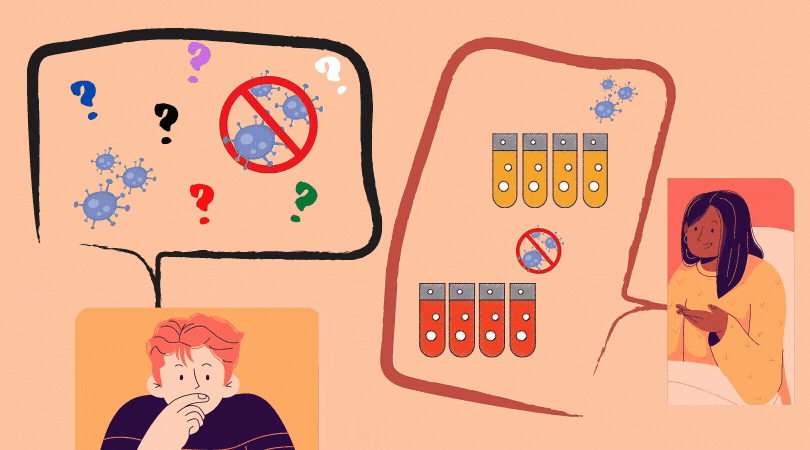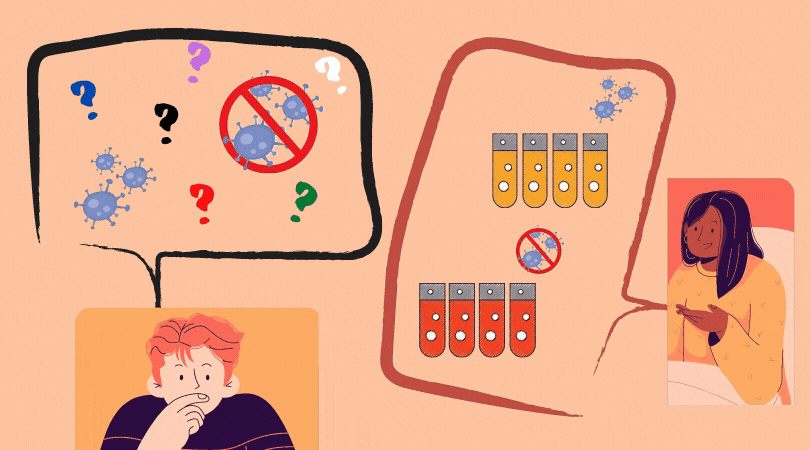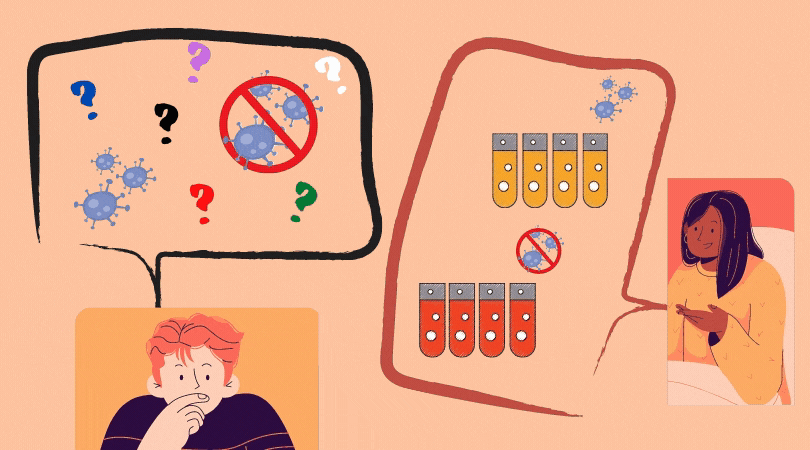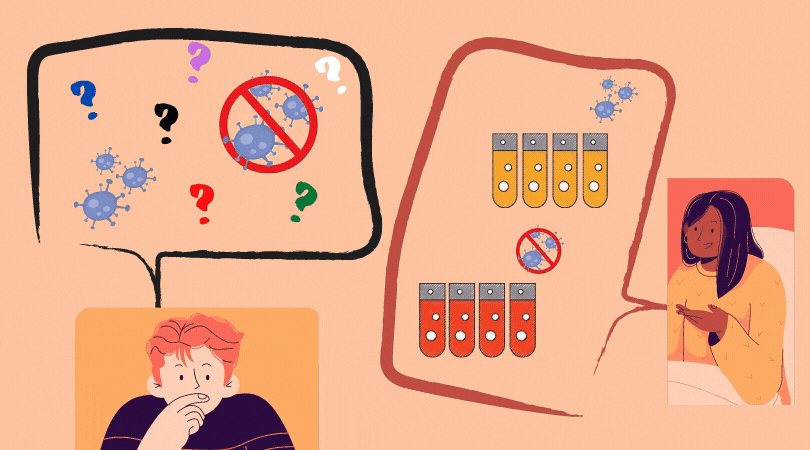
Primeiro, você precisa saber que, pra funcionar, o biossensor atua na presença de Angiotensina II – que será adicionado ao CORONAYEAST da mesma forma que “tampões de corrida” são adicionadas ao teste rápido – ou seja, um conjunto de reagentes que permite que a reação ocorra e o sinal seja visível. Vamos pensar então nos dois cenários: a levedura na presença e ausência do vírus.
Na ausência do vírus, a levedura modificada está em um meio contendo uma concentração conhecida de Angiotensina II. Neste cenário, o ACE2 está disponível para converter a Angiotensina II em Angiotensina 1-7, diminuindo a concentração do primeiro. Desta forma, o AT1 não será ativado, uma vez que seu receptor – a Angiotensina II – não estará lá. Receptor não ativado: gene repórter não produzido e levedura não muda de cor.
Na presença do vírus, a alta afinidade que a proteína Spike do SARS-CoV-2 possui com a ACE2 faz com que sua atividade enzimática fique comprometida. Desta forma, quanto mais vírus, menos ACE2 disponível. Logo: Angiotensina II acumula no meio extracelular, uma vez que a ACE2 está “ocupada” com o SARS-CoV-2, ou, em termos biológicos: a função enzimática de conversão em Angiotensina 1-7 foi capturada pelo vírus. Isto quer dizer que: mais Angiotensina II no meio extracelular significa maior a ativação do receptor AT1.
É aqui que entra o resultado da nossa pesquisa! Na presença do vírus, portanto, o receptor AT1 ativado da levedura modificada geneticamente emitiria um sinal que faria o gene repórter ativar e produzir uma proteína que faria a levedura mudar de cor: fluorescente ou vermelha, a olho nu.
– Nossa! Que legal! Eu estou com suspeita de COVID-19, onde posso fazer este teste diagnóstico?
– Calma! O CORONAYEAST ainda está sendo desenvolvido pelo LGE!
Benefícios da pesquisa, caso os resultados sejam positivos
Uma vez que o CORONAYEAST estiver pronto e funcional, seus benefícios serão extensos. Vamos falar um pouco disso agora…
Primeiro, o preço. Imagine a diferença de custo entre produzir um diagnóstico dependente de insumos importados e infraestrutura especializada (como é o caso do qRT-PCR) e um teste em que um microorganismo faz tudo. A levedura cresce fácil – coloque um pouco de açúcar e pronto. Sem contar que o Brasil tem uma infraestrutura bastante robusta para isso. Isto é, já produzimos bastante desse fungo para usarmos na produção de etanol, por exemplo. E o diagnóstico só dependeria dela, a S. cerevisiae modificada (com um pouco de Angiotensina II). Estimamos custo de produção até 100 vezes menor que para o teste de PCR!
Outra vantagem importante é a especificidade. Como falamos, a detecção do SARS-CoV-2 é permeada por um GPCR e, por isso, é bastante específica. A única possibilidade de se alterar o sinal captado pelo AT1 é a ligação do vírus com ACE2. Aliás, usarmos a ACE2 também é outra garantia de especificidade, porque sabemos que esta é a única forma que o coronavírus da covid-19 reconhece uma célula hospedeira. Também não prevemos a alteração da funcionalidade desta enzima por qualquer outro composto presente na saliva. Esta é uma característica do CORONAYEAST que o coloca à frente dos atuais testes rápidos, porque sabemos o quanto estes têm altas taxas de resultados falsos.
Ademais, o diagnóstico para Covid-19 a partir do biossensor baseado em levedura detecta o vírus inteiro. Isso quer dizer que 1) não precisamos extrair material genético viral, como o teste de PCR; 2) não é baseado em anticorpos, como nos atuais testes rápidos imunológicos, permitindo identificar potenciais vetores da doença, ainda que assintomáticos; 3) poderia ser usado em superfícies para teste da presença do vírus, permitindo a correta desinfecção de ambientes. CORONAYEAST se apresenta como um conceito disruptivo e inovador que está sob atual desenvolvimento e poderá mudar a forma como fazemos diagnósticos virais!
E sabe o que é mais interessante de tudo isto? É tecnologia brasileira, pesquisa nacional, feita por cientistas do nosso país. Barateando o custo para diagnóstico e o tempo de resposta do resultado.
Este texto foi elaborado a partir de uma pesquisa financiada pela FAPESP, cujo processo é n.2018/03403-2
Força Tarefa da Unicamp
O artigo que embasou esta postagem faz parte de um conjunto de postagens sobre as pesquisas científicas que a Unicamp vem fazendo desde o início da pandemia, no que chamamos “Força Tarefa”. O Especial Covid-19, do Blogs de Ciência da Unicamp, participa da Força Tarefa desde o início, com a divulgação científica sobre a doença. Mas também vai se dedicar à publicação destes conhecimentos produzidos especificamente pelos pesquisadores da Unicamp cada vez mais! Acompanhe as próximas postagens!
Nossos sites institucionais:
Para Saber mais
Chauhan DS, Prasad R, Srivastava R et al. Comprehensive Review on Current Interventions, Diagnostics, and Nanotechnology Perspectives against SARS-CoV-2. Bioconjug Chem 2020:acs.bioconjchem.0c00323.
Nakamura, Y., Ishii, J. and Kondo, A. (2014), Construction of a yeast‐based signaling biosensor for human angiotensin II type 1 receptor via functional coupling between Asn295‐mutated receptor and Gpa1/Gi3 chimeric Gα. Biotechnol. Bioeng., 111: 2220-2228. doi:10.1002/bit.25278
Tang Y-W, Schmitz JE, Persing DH et al. Laboratory Diagnosis of COVID-19: Current Issues and Challenges. McAdam AJ (ed.). J Clin Microbiol 2020;58:e00512-20.
Os Autores
Ana Arnt é Bióloga, Mestre e Doutora em Educação. Professora do Departamento de Genética, Evolução, Microbiologia e Imunologia, do Instituto de Biologia (DGEMI/IB). Pesquisa e da aula sobre História, Filosofia e Educação em Ciências, e é uma voraz interessada em cultura, poesia, fotografia, música, ficção científica e… ciência!
Carla Maneira da Silva Mestranda em Genética de Micro-organismos pela Universidade Estadual de Campinas (UNICAMP). Realiza suas atividades de pesquisa no Laboratório de Genética e Bio-Energia (LGE). Possui experiência na área de genética e engenharia metabólica. Mais especificamente na produção de compostos de interesse econômico a partir de micro-organismos. Assim como na produção de biossensores baseados em levedura.
Fellipe Mello é Engenheiro químico (2014) e doutor em ciências (2019) pela Universidade Estadual de Campinas. Atualmente é post doc em engenharia genética no Laboratório de Genômica e bioEnergia no Instituto de Biologia da Unicamp. Tem experiência na área de engenharia química, com ênfase em termofluidodinâmica, no reaproveitamento de biomassas e purificação de proteínas; e na área de genética, com ênfase em engenharia metabólica e estudo de QTLs.
Este texto é original e escrito com exclusividade para o Especial Covid-19



0 comentário