Por que estudar química?
Imagem de Shutterstock
– Texto de Roberto Costa
Tabela periódica, cadeia de carbono, átomos. Para muita gente, essas palavras assustam. Estudar química pode parecer complicado à primeira vista, mas quando começamos a relacionar a ciência ao nosso cotidiano o estudo pode se tornar muito mais natural e prazeroso.
Química é a ciência que estuda a estrutura das substâncias, a composição e as propriedades das diferentes matérias, suas transformações e variações de energia. Na prática, isso quer dizer que o papel da química da nossa vida é muito importante. Indústria alimentícia, petroquímica, farmacêutica, têxtil e outras dependem diretamente da química, assim como a criação de novos medicamentos e materiais biodegradáveis.
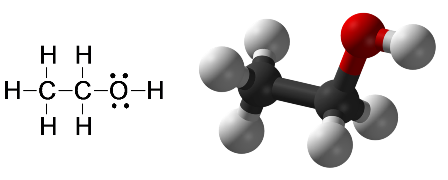
Ela faz parte do nosso dia-a-dia. O simples fato de estarmos vivos indica que reações químicas estão acontecendo dentro de nós, o tempo todo. A nossa respiração é pura química, e todas as atividades diárias envolvem química. Cada cheiro que sentimos demanda uma série de reações químicas intra-neuroniais. Acetona, álcool, grafite… Esses termos comuns do dia a dia também fazem parte do repertório da química.
Aprendendo química, é possível entender melhor o mundo ao seu redor. Com ela você fica sabendo porque o detergente retira a gordura, porque as folhas mudam de cor no outono e como a cerveja é produzida, por exemplo. Com ela, você entende os rótulos de produtos e pode até aprender a cozinhar melhor!
Além disso, ela é importante para compreender outras disciplinas, como Biologia, Ciências Ambientais, Física, Medicina e Ciências da Saúde. É por interligar tudo isso que a química é chamada de “ciência central”.
E atenção: se você se apaixonar pela química, ela é também uma ótima opção profissional. Entre as atribuições de um químico estão a elaboração de projetos de instalações industriais, manutenção de equipamentos, pesquisa e criação de novos materiais, controle e supervisão da produção e aplicação de testes de qualidade.
O momento para seguir nesta área não poderia ser melhor. A Associação Brasileira da Indústria Química (Abiquim) estima que os investimentos na indústria química brasileira devem chegar a 167 bilhões de dólares até 2020 e criar mais de 2 milhões de empregos. Segundo o Guia do Estudante, entre os melhores cursos de química estão o da Universidade de Brasília (UnB), Universidade Federal de Minas Gerais (UFMG), Universidade Federal do Paraná (UFPR), Pontifícia Universidade Católica do Rio de Janeiro (PUC-Rio), Universidade Federal do Rio de Janeiro (UFRJ) e Universidade Federal do Rio Grande do Sul (UFRGS).
Para quem já embarcou nos estudos mas enfrenta dificuldades, uma boa dica é buscar informações complementares na internet. Algumas ferramentas são gratuitas e podem ser muito úteis, como o PasseiDireto, rede social acadêmica onde é possível trocar conhecimento e compartilhar arquivos com outros estudantes universitários, de diversas instituições do país, públicas e privadas.
Roberto Costa, formando de jornalismo que ama pesquisas científicas.
Fontes:
http://quimicaouniversoemmovimento.blogspot.com.br/
http://www.abiquim.org.br/home/associacao-brasileira-da-industria-quimica
http://passeidireto.com/
Fim de jogo


Rindo de que ou de quem?

Síntese de proteínas: um épico no nível celular*

Do modelo à realidade?


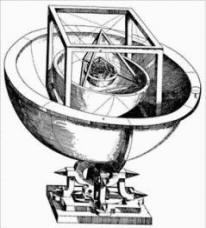
Primeiro vieram os astrônomos, observando os movimentos dos corpos celestes e coletando dados. Em segundo lugar vieram os matemáticos, inventado a notação matemática para descrever os movimentos e ajustar os dados. Em terceiro vieram os técnicos, fazendo modelos mecânicos para simular aquelas construções matemáticas. Em quarto vieram gerações de estudantes, que aprenderam sua astronomia a partir dessas máquinas. Em quinto vieram cientistas, cuja imaginação estava tão ofuscada por gerações de tal aprendizado que de fato acreditam que era daquele modo que os céus se comportavam. Em sexto vieram as autoridades, que defendiam o dogma estabelecido. E assim a raça humana foi induzida a aceitar o Sistema Ptolomaico por cerca de um milênio.



Uma luz dentro de células

Por Joey Salgado
A Fernanda Poletto, do excelente Bala Mágica, publicou recentemente um texto falando sobre Armas Mágicas (quanta mágica por aqui…), o qual recomendo fortemente a leitura. O conceito de Armas Mágicas se resume a uma metodologia capaz de promover a internalização de fármacos em tumores, através da utilização de peptídeos chamados de iRGD. Os iRGD “guiam” o fármaco até o tumor e “abrem a porta” para que o mesmo entre na célula tumoral, aumentando assim a especificidade de sua ação.
Achei sensacional a utilização desses peptídeos iRGD para o carregamento do fármaco e, por conta disso, recordei-me de um trabalho relativamente recente (2006 tá novo ainda?), onde uma certa sequência de peptídeos mostrou-se fundamental para a proposta de uma nova técnica. Em 2006 (quatro anos… tá novo, foi a menos de uma Copa do Mundo atrás…), Jones e colaboradores, da Universidade de Standford (sempre eles…) demonstraram a possibilidade de se utilizar oligopeptídeos contendo oito resíduos de arginina como cross-coupling peptides (ou CCP) de moléculas conjugadas com luciferina (lembra dela?). O princípio da técnica é demonstrado na figura abaixo.[1]
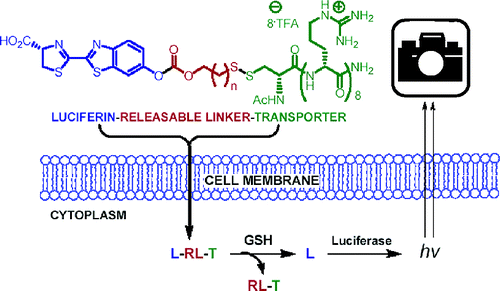
Vamos por partes. Oligopeptídeos de arginina, principalmente esses contendo oito unidades desse aminoácido, são chamados de cross-coupling peptides justamente por possuírem a capacidade de permearem através da membrana lipofílica de células, chegando ao citoplasma da mesma. A subunidade em verde da molécula na figura acima diz respeito à sequência de CPPs. Pelo fato de permearem por membranas lipofílicas, ao mesmo tempo que são solúveis em meio aquoso, CPPs podem ser conectados a outros peptídeos, fármacos ou agentes marcadores, formando os chamados “conjugados”, que podem ser carregados para dentro de uma célula. Já na época do trabalho, o mesmo grupo de pesquisas havia apresentado a utilização de CPPs conjugados com ciclosporina A, um imunossupressor, para “entrega” de drogas em tecidos vivos.[2] O problema, de certa forma, é que a velocidade com que a entrega do fármaco era realizada, ou de qualquer outra molécula conjugada ao CPP, era desconhecida até então. Sabia-se que o CPP realizava a entrega, visto que os efeitos do fármaco eram observados, mas não se tinha ideia de quanto tempo era necessário para o mesmo permear para dentro da célula e/ou para liberar o fármaco.
No sentido de se desenvolver uma técnica que permitisse avaliar a eficiência e a velocidade da “entrega” de um determinado conjugado com CPP, em tempo-real e in vivo, chegou-se a conjugados de CPP com luciferina, como já demonstrado na figura acima. A luciferina (destacada em azul) está conectada ao CPP (em verde) através de uma molécula-ponte (em vermelho). Tal molécula-ponte está conectada ao CPP por uma ligação disulfeto S-S (em vermelho e verde), que quando na presença de glutationa intracelular (GSH) é rapidamente clivada, liberando a molécula de luciferina. Utilizando-se tal conjugado em células de organismos transfectados com o gene luc de vaga-lumes, responsável pela expressão da enzima luciferase, o par luciferina/luciferase emite luz, que pode ser registrada em tempo-real por uma câmera.
Dessa forma, mostrou-se ser possível averiguar a eficiência e a velocidade de permeação de CPPs de arginina, utilizando-se esse conjugado com luciferina como modelo para entrega intracelular de drogas. Apesar do sucesso obtido pelos autores, parte da complicação em se utilizar tal técnica reside na síntese do conjugado, que não é trivial, e no fato de que devem ser utilizados organismos geneticamente modificados para avaliação do modelo. Contudo, a técnica equivalente, que utiliza CPPs conjugados com moléculas fluorescentes, apesar de possibilitar que se faça a avaliação da liberação de drogas in vitro, não é funcional para sistemas in vivo e não permite o acompanhamento da mesma em tempo-real. Outra opção, o uso de CPPs conjugados com moléculas contendo radioisótopos, possibilita a observação in vivo, mas não tem resolução suficiente para determinar se o conjugado marcado se encontra dentro ou fora da célula e não permite saber se a molécula marcada que simula o fármaco ainda está ligada ao CPP (o radioisótopo emite radiação independente se foi liberado dentro do meio celular ou não).
Este é um exemplo de um belo trabalho, na minha opinião, que apresenta uma técnica fenomenal, capaz de modelar em tempo-real a entrada em células de drogas conjugadas a CPPs, e que ao mesmo tempo permite as observações da liberação intracelular da mesma e da interação com um receptor enzimático.
Que beleza esses peptídeos, né não?!
Referências e notas:
[1] Jones, L. R.; GOun, E. A.; Shinde, R.; Rothbard, J. B.; Contag, C. H.; Wender, P. A.; “Releasable Luciferin-Transporter Conjugates: Tools for the Real-Time Analysis of Cellular Uptake and Release” J. Am. Chem. Soc. 2006, 128, 6526. DOI: 10.1021/ja0586283.
[2] Rothbard, J. B.; Garlington, S.; Lin, Q.; Kirschberg, T.; Kreider, E.; McGrane, P. L.; Wender, P. A.; Khavari, P. A.; “Conjugation of arginine oligomers to cyclosporin A facilitates topical delivery and inhibition of inflamation” Nat. Med. 2000, 6, 1253. DOI: 10.1038/81359.
Que se faça a luz!

Por Joey Salgado












