Para que Bala Mágica? Use logo uma ARMA mágica, oras!
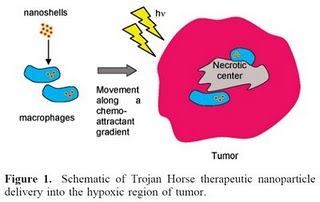
A proposta do nome Arma Mágica é recente, embora a ideia em si seja mais antiga. Seu argumento é baseado no fato de que o acúmulo do fármaco na região de vascularização do tumor em comparação com as demais regiões do corpo não significa necessariamente que ocorrerá uma distribuição eficiente do fármaco DENTRO do tumor. Note que esses conceitos realmente são diferentes. Lembra do efeito EPR? Se você tem fármaco encapsulado dentro de nanopartículas, e essas nanopartículas que circulam pelo sangue passam por uma região de tumor, elas se acumulam nesse local porque “escapam” da corrente sanguínea devido ao aumento dos espaços entre as células dos vasos da região tumoral – esse aumento localizado da permeabilidade dos vasos sanguíneos garante o acúmulo na superfície do tumor, mas não garante que as nanopartículas penetrarão profundamente nele.
É nesse ponto da história que entram peptídeos contendo a seqüência de aminoácidos arginina-glicina-aspartato. Tais peptídeos são capazes de se ligarem a integrinas (uma família de receptores celulares) presentes tanto no endotélio quanto no parênquima da região tumoral. Há dois tipos, o RGD e o iRGD. Cada letra corresponde a um aminoácido. O i do nome quer dizer que o peptídeo é quebrado depois de se ligar à integrina de um jeito tal que resulta na perda da sua afinidade com a dita integrina e ganho da afinidade por um outro receptor de membrana chamado neuropilina-1 (NRP-1). Quando uma molécula se liga à NRP-1, vai para dentro da célula. Nesse caso, a NRP-1 é como uma porta – para entrar é preciso se ligar a ela, ou melhor, girar a maçaneta. Dessa forma, o RGD pode ser usado para direcionar o fármaco para o local do tumor, mas o iRGD tem a vantagem de direcioná-lo E internalizá-lo.
Fármacos quimicamente ligados a peptídeos iRGD podem ser internalizados no tecido do tumor através desse um mecanismo ativo de endocitose, garantindo uma maior eficácia do tratamento (que ainda está em fase de estudo, não há tal tratamento disponível para a população ainda). Mas o mais interessante na minha humilde opinião é que o fármaco pode ser internalizado sem estar quimicamente ligado ao iRDG. Basta que ambos sejam administrados ao mesmo tempo. Isso é vantajoso porque às vezes modificações químicas na estrutura do fármaco podem comprometer sua atividade biológica. A co-administração do iRGD com nanopartículas contendo o fármaco também teve o mesmo efeito de aumento da eficácia biológica. O nanoencapsulamento se justifica no caso de fármacos com baixa afinidade pela água, pois pode reduzir efeitos adversos do tratamento por evitar o uso de co-solventes. Embora a ideia pareça realmente bastante promissora, ainda há muitas perguntas a serem respondidas quanto ao uso de seqüências iRGD para esse fim. Afinal, testes clínicos ainda não foram feitos, e o que vale para animais de laboratório pode não se repetir tão bem em humanos. É preciso verificar, a partir de estudos clínicos, se efeitos tóxicos não poderiam ser exacerbados pela ligação do iRGD a locais não-tumorais contendo integrinas. E isso não vale só para estudos envolvendo iRGD, mas para todos aqueles que utilizam a estratégia ligante-receptor (também conhecida como vetorização ativa).
Moral da história: renomear uma ideia que não é completamente nova com um nome chamativo e descolado dá o maior ibope.
OBS.: O tema foi dica do Takata
Feron, O. (2010). Tumor-Penetrating Peptides: A Shift from Magic Bullets to Magic Guns Science Translational Medicine, 2 (34), 34-34 DOI: 10.1126/scitranslmed.3001174
Sugahara, K., Teesalu, T., Karmali, P., Kotamraju, V., Agemy, L., Girard, O., Hanahan, D., Mattrey, R., & Ruoslahti, E. (2009). Tissue-Penetrating Delivery of Compounds and Nanoparticles into Tumors Cancer Cell, 16 (6), 510-520 DOI: 10.1016/j.ccr.2009.10.013
Sugahara, K., Teesalu, T., Karmali, P., Kotamraju, V., Agemy, L., Greenwald, D., & Ruoslahti, E. (2010). Coadministration of a Tumor-Penetrating Peptide Enhances the Efficacy of Cancer Drugs Science, 328 (5981), 1031-1035 DOI: 10.1126/science.1183057
Quando a desunião pode ajudar a salvar vidas
Intrigado com o título do post?
Antes que elucubrações filosóficas surjam na sua mente, esclareço que a desunião à qual me refiro é de células. Células? Sim, das células que recobrem a parede dos vasos sanguíneos. O conjunto dessas células é chamado de epitélio endotélio (update 10/11/09: termo gentil e devidamente corrigido pelo Gabriel). Em tecidos sadios, essas células são bem próximas umas das outras. Apenas pequenas moléculas podem atravessar os espaços entre elas, passando do sangue para os tecidos vizinhos. No entanto, em regiões inflamadas ou mesmo em regiões atacadas por tumores, essas células estão menos unidas entre si que aquelas de regiões sadias.
 (Origem da imagem: aqui)
(Origem da imagem: aqui)
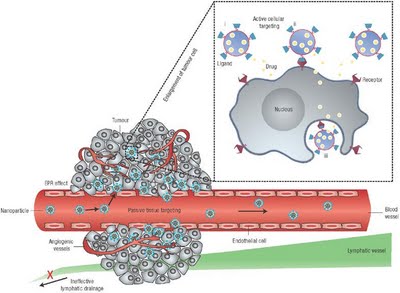
Pense comigo: se as nanopartículas passam apenas pela parede dos vasos nas regiões com tumor, a consequência é um acúmulo das nanopartículas no tecido tumoral vizinho ao vaso sanguíneo, certo? O pessoal da área de nanobiotecnologia chama essa estratégia de vetorização de efeito EPR (sigla em inglês que significa permeabilidade e retenção aumentados). A ilustração acima mostra como ocorre acúmulo de nanopartículas em regiões tumorais devido ao efeito EPR.
Nano-kit de análises clínicas

(créditos: Bi e col., 2009 – Biosensors and Bioelectronics)
Anticorpos também foram ligados na superfície de nanopartículas magnéticas. Na presença de uma proteína no soro que só existe quando a pessoa tem câncer (é o que chamamos de biomarcador), o nanotubo e a nanopartícula magnética se juntam e reações químicas passam a acontecer nesse sanduíche nanotecnológico. O nanotubo e a nanopartícula magnética são capazes de se juntar porque os anticorpos de ambos se ligam nessa proteína biomarcadora
No estudo em questão, os autores usaram como proteína marcadora a alfa-fetoproteína (AFP), que corresponde à bolinha azul no esquema acima. Quando uma mistura de H2O2, azul de bromofenol (um tipo de corante) e luminol (aquele mesmo, do seriado CSI) é adicionada ao soro do paciente com câncer e, nessa mistura, os nanotubos e as nanopartículas magnéticas são adicionados também, ocorre luminescência devido à ação da enzima peroxidase na superfície do nanotubo, que quebra a H2O2. Os produtos da quebra da H2O2 reagem com o luminol e o azul de bromofenol emitindo luz, mas só na presença de metal – no caso, a nanopartícula magnética. Se o paciente não tem câncer, seu soro não terá a proteína biomarcadora. Sem proteína biomarcadora não ocorre ligação da nanopartícula magnética com o nanotubo que contém a peroxidase. Portanto, sem proteína marcadora no soro não há emissão de luz.
Esse sanduíche nanotecnológico conseguiu detectar quantidades de proteína marcadora de câncer no soro que outros testes padrão (como o ELISA) não conseguiram. Pequeno tamanho, grande sensibilidade!
Bi, S., Zhou, H., & Zhang, S. (2009). Multilayers enzyme-coated carbon nanotubes as biolabel for ultrasensitive chemiluminescence immunoassay of cancer biomarker Biosensors and Bioelectronics, 24 (10), 2961-2966 DOI: 10.1016/j.bios.2009.03.002
Os aviões Stealth do nano(bio)mundo
 (fonte: http://www.atfx.org/photos/f117a.jpg)
(fonte: http://www.atfx.org/photos/f117a.jpg)
Melanoma: um alerta a todos (PARTE II)
Aliás, já disse alguém que se fossemos camundongos não morreríamos nunca, de tanto que já se estudou a cura de doenças nesses animais…..
É claro que esses ainda são só dois exemplos de estudos acadêmicos, mas quem sabe a próxima geração possa aproveitar os frutos da nanobiotecnologia e não precise passar por uma cirurgia de remoção do melanoma como a que me submeti, ou mesmo à severidade da quimioterapia tradicional em casos mais graves.
Lu, W., Xiong, C., Zhang, G., Huang, Q., Zhang, R., Zhang, J., & Li, C. (2009). Targeted Photothermal Ablation of Murine Melanomas with Melanocyte-Stimulating Hormone Analog-Conjugated Hollow Gold Nanospheres Clinical Cancer Research, 15 (3), 876-886 DOI: 10.1158/1078-0432.CCR-08-1480
Villares, G., Zigler, M., Wang, H., Melnikova, V., Wu, H., Friedman, R., Leslie, M., Vivas-Mejia, P., Lopez-Berestein, G., Sood, A., & Bar-Eli, M. (2008). Targeting Melanoma Growth and Metastasis with Systemic Delivery of Liposome-Incorporated Protease-Activated Receptor-1 Small Interfering RNA Cancer Research, 68 (21), 9078-9086 DOI: 10.1158/0008-5472.CAN-08-2397
Melanoma: um alerta a todos (PARTE I)
 (fonte: http://www.ilhagrande.org/Praia-Camiranga)
(fonte: http://www.ilhagrande.org/Praia-Camiranga)“A Sra. tem melanoma maligno, está indicado aqui na biópsia”.
“Caramba! Mas eu só tenho 28 anos, nem pego tanto sol assim, como é que pode?”
Tanto pode que aconteceu. E eu tive muita sorte de detectá-lo no início, porque o melanoma é o câncer de pele mais grave devido à sua alta possibilidade de metástase. E eu que achava que era só uma pinta….
De acordo com o site do INCA, órgão do Ministério da Saúde do Brasil, deve-se suspeitar da transformação de uma pinta em melanoma quando ocorre um aumento no seu tamanho e uma alteração na sua coloração e forma (ela passa a ter bordas irregulares). Quando há metástase, o melanoma é incurável na maioria dos casos. Porém, quando os melanomas são detectados no início, são curáveis. A cirurgia é o tratamento mais indicado. Nessa cirurgia, retira-se não só a lesão, mas um bom pedaço de pele ao redor, para garantir. É como queijo com fungo em uma das bordas. Para aproveitar o resto bom, tira-se o pedaço com fungos mais uma “margem de segurança”.
Fiquei pensando se não haveria alguma alternativa à cirurgia (imaginem, por exemplo, se o melanoma aparece no rosto – a cicatriz resultante não é nada legal) ou tratamentos mais efetivos para os casos mais graves e encontrei alguns estudos (ainda em fase inicial) interessantes sobre o uso de nanobiotecnologia para a cura do melanoma.
O pulo-do-gato que permitiu curar câncer usando remédio para artrite
Já havia sido demonstrado antes que a indometacina poderia matar as células cancerosas responsáveis pelo glioma em plaquinhas no lab. No entanto, nunca se soube de ninguém que tenha tomado indometacina até hoje e tenha se curado dessa doença, que pode causar convulsões, dor de cabeça, vômitos em jato, parestesias e hemianospia.
O estudo em questão mostrou que, quando a indometacina é incorporada nessas nanocápsulas, ela adquire a capacidade de atravessar a barreira entre o sangue e o cérebro. Esse foi o pulo-do-gato. Ao chegar no cérebro de ratos, a indometacina nanoencapsulada causou uma redução no tamanho dos tumores cerebrais. A indometacina pura, ao contrário, não fez nem cócegas. O primeiro grupo de ratos, que recebeu as nanocápsulas, viveu muito mais tempo que os outros grupos. Hoje em dia, o tratamento quimioterápico de gliomas causa muito sofrimento aos pacientes e seus benefícios são mínimos. O que se faz é retirar o tumor com cirurgia para descomprimir o cérebro e aliviar a hipertensão intracraniana. O problema é que quase sempre é impossível retirar todas as células afetadas e o câncer volta. Esse estudo abre uma nova perspectiva de tratamento quimioterápico de gliomas sem efeitos colaterais mais graves (os efeitos colaterais seriam os mesmos que os de outros remédios contendo indometacina).
Parabéns aos autores pelo excelente trabalho!
P.S.: Saliento que esse é um estudo em fase pré-clínica (ou seja, em animais). Ainda há muito chão antes de um medicamento como esse chegar ao mercado.
Glossário
Parestesias: são sensações subjetivas da pele (ex., frio, calor, formigamento, pressão, etc.) que são vivenciadas espontaneamente na ausência de qualquer estímulo externo.
Hemianospia: perda da visão em metade ou um quarto do campo visual.
Referencia:
Bernardi, A., Braganhol, E., Jäger, E., Figueiró, F., Edelweiss, M., Pohlmann, A., Guterres, S., & Battastini, A. (2009). Indomethacin-loaded nanocapsules treatment reduces in vivo glioblastoma growth in a rat glioma model Cancer Letters, 281 (1), 53-63 DOI: 10.1016/j.canlet.2009.02.018
Uma diferença que pode auxiliar na cura e diagnóstico do câncer
 Créditos: Sokolov Group, Clarkson University
Créditos: Sokolov Group, Clarkson University
Iyer, S., Gaikwad, R., Subba-Rao, V., Woodworth, C., & Sokolov, I. (2009). Atomic force microscopy detects differences in the surface brush of normal and cancerous cells Nature Nanotechnology, 4 (6), 389-393 DOI: 10.1038/nnano.2009.77