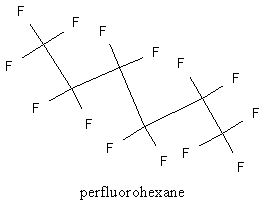
Perfluorohexano (flúor em todas direções)
Todos sabem que muitos solventes orgânicos não se misturam com água (ou, de forma mais geral, alguns solventes polares são se misturam com solventes não-polares). O que talvez você não saiba é que alguns líquidos altamente fluorados não são muito polares, mas mesmo assim não se dissolvem em água ou em muitos orgânicos.
De fato, você pode misturar certos solventes orgânicos, a substância fluorada, e água, e acabará com três fases! A empresa indicada neste link trabalha usando marcadores perfluorinados para agregar em sua molécula, que por sua vez se fixa em um suporte sólido perfluorinado (você pode posteriormente lavar seu produto com algo que interage com esses marcadores fluorados).
A 3M vende uma mistura de hidrocarbonetos leves fluorados conhecidos como “fluorinert” que incluem moléculas como a acima. A bizarrice do flúor dá a característica destes compostos – não somente suas características de solubilidade são únicas, eles são realmente estáveis graças à ligação forte carbono-flúor, fazendo deles um dos raros haletos de alquila que não são tóxicos – é até mesmo possível respirá-los!
http://scienceblogs.com/moleculeoftheday/2008/01/perfluorohexane_it_hates_every.php
Original (English) content from Molecule of the Day (http://scienceblogs.com/moleculeoftheday). Content translated with permission, but portuguese text not reviewed by the original author. Please do not distribute beyond this site without permission from both author and translator.







Discussão - 0 comentários