Ácido carmínico (comendo insetos)
Esta sempre choca as pessoas na primeira vez em que escutam sobre isso. Você já viu escrito ´carmim´ em algum rótulo de alimento com uma cor vermelho-púrpura? Sim, você está comendo insetos.
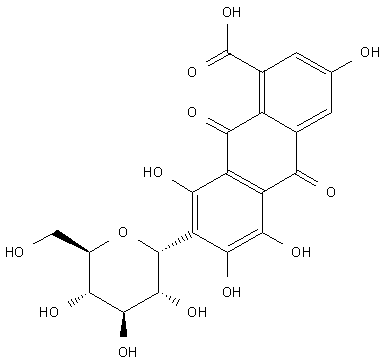
O ácido carmínico é extraído da carapaça de alguns insetos.
E você não está necessariamente seguro se não disser ´carmim´ – o composto pode estar escondido em um apelido tranquilizador como ´ingredientes naturais´ – que os fabricantes de alimentos começaram a usar por causa do receio dos corantes artificiais!
http://scienceblogs.com/moleculeoftheday/2008/01/carminic_acid_no_seriously_you.php
Original (English) content from Molecule of the Day (http://scienceblogs.com/moleculeoftheday). Content translated with permission, but portuguese text not reviewed by the original author. Please do not distribute beyond this site without permission from both author and translator.
Ácido oxálico (problema para os rins)
Um texto sobre cetona de framboesa me fez pensar sobre os suplementos alimentares em geral. A maior parte deles não causa problemas – o que é bem interessante, considerando que muitos deles tem coisas parecidas com medicamentos. A maior parte das pessoas estão utilizando sem nenhuma supervisão, e somente o rótulo os guia.
Existem diversas coisas tóxicas nas plantas. Um de tais compostos é o ácido oxálico, que as plantas toleram bem, mas os mamíferos nem tanto.
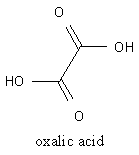
O grande problema com o oxalato é que ele faz um belo trabalho na coordenação com cátions metálicos divalentes, formando complexos insolúveis. Oxalato de cálcio pode precipitar em seus rins, formando pedra nos rins.
A mesma rota metabólica no seu corpo que processa o etanol irá processar o etilenoglicol – um anticongelante – até ácido oxálico – daí sua toxicidade. Por esta razão, algumas pessoas começaram a usar propileno glicol, que é metabolizado até o inocente piruvato (que na verdade serve como nutriente!).
Suas enzimas de processamento de álcool fazem um trabalho melhor no etanol do que em qualquer outra coisa (nós evoluímos em presença de pequenas quantidades de etanol). Por causa disso, o etanol é um antídoto para o envenenamento com etilenoglicol – e os médicos de emergência costumavam deixar você bêbado nestas situações. Agora existe um antídoto melhor, então acho que você não verá mais bebedeiras na sala de emergência.
Veja um texto antigo para mais informações sobre o metabolismo de oxalato e etilenoglicol.
http://scienceblogs.com/moleculeoftheday/2008/01/oxalic_acid_the_painful_fate_o.php
Original (English) content from Molecule of the Day (http://scienceblogs.com/moleculeoftheday). Content translated with permission, but portuguese text not reviewed by the original author. Please do not distribute beyond this site without permission from both author and translator.
Vidro de urânio

O vidro de urânio é uma daquelas raras belezas perdidas no tempo. O temor pela radioatividade inibe o interesse de alguém querer beber um vinho em uma taça com este tipo de material, mesmo que a radioatividade seja baixa e praticamente inofensiva.
O vidro de urânio contém o material na forma de óxido diuranato, em uma faixa que pode variar de 2% até 25%. A cor pode variar entre o amarelo e o esverdeado dependendo do estado de oxidação e da concentração dos íons metálicos, e de outros tipos de aditivos. O espetáculo de cores ocorre quando se incide luz ultravioleta sobre o material, que imediatamente adquire um curioso brilho esverdeado.
Veja o brilho de uma bolita ao se incidir luz UV de um laser de blu-ray.


Livros sobre o assunto

Mais informações em
http://en.wikipedia.org/wiki/Uranium_glass
Leia também
Trinitita – mineral gerado em uma explosão nuclear
Perfluorohexano (flúor em todas direções)
Todos sabem que muitos solventes orgânicos não se misturam com água (ou, de forma mais geral, alguns solventes polares são se misturam com solventes não-polares). O que talvez você não saiba é que alguns líquidos altamente fluorados não são muito polares, mas mesmo assim não se dissolvem em água ou em muitos orgânicos.
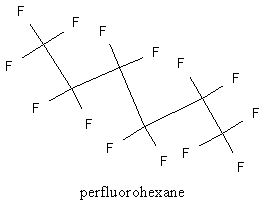
De fato, você pode misturar certos solventes orgânicos, a substância fluorada, e água, e acabará com três fases! A empresa indicada neste link trabalha usando marcadores perfluorinados para agregar em sua molécula, que por sua vez se fixa em um suporte sólido perfluorinado (você pode posteriormente lavar seu produto com algo que interage com esses marcadores fluorados).
A 3M vende uma mistura de hidrocarbonetos leves fluorados conhecidos como “fluorinert” que incluem moléculas como a acima. A bizarrice do flúor dá a característica destes compostos – não somente suas características de solubilidade são únicas, eles são realmente estáveis graças à ligação forte carbono-flúor, fazendo deles um dos raros haletos de alquila que não são tóxicos – é até mesmo possível respirá-los!
http://scienceblogs.com/moleculeoftheday/2008/01/perfluorohexane_it_hates_every.php
Original (English) content from Molecule of the Day (http://scienceblogs.com/moleculeoftheday). Content translated with permission, but portuguese text not reviewed by the original author. Please do not distribute beyond this site without permission from both author and translator.
Propofol (leite de amnésia)
Anestésicos são estranhos. Muitos do que nós usamos tem uma escassez de oxigênio e nitrogênios que parecem fazer muitos dos medicamentos funcionarem, e tem sido um desafio substancial e uma preocupação em saber como essas coisas funcionam. O xenônio, por exemplo, é um bom anestésico que é, é claro, composto de um único átomo. Similarmente, moléculas altamente halogenadas, que fora isso são sem muitos atrativos, são comuns.
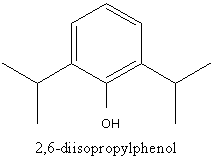
Propofol é usada em uma emulsão IV (uma íntima mistura de água e óleo, tal como molho ranch dressing, ou GOJO). A cor leitosa do produto é a origem de seu apelido no título – “Leite de Amnésia”. O método de administração é em grande parte por razões de solubilidade, mas mas as emulsões podem fazer mais do que solubilizar coisas teimosas. A benéfica melatonina que você toma para jet lag, quando administrada em altas doses em uma emulsão, pode atuar como um forte anestésico mais do sua origem, em lojas de produtos naturais, poderia sugerir.
http://scienceblogs.com/moleculeoftheday/2007/12/propofol_milk_of_amnesia.php
Original (English) content from Molecule of the Day (http://scienceblogs.com/moleculeoftheday). Content translated with permission, but portuguese text not reviewed by the original author. Please do not distribute beyond this site without permission from both author and translator.
Ácido bongkrek (nome engraçado, resultados nem tanto)
Em muitas partes do mundo, o que o mundo Ocidental chamaria de “alternativas à carne” são a principal fonte de proteína. Um de tais produtos é o tempeh, feito de soja. Uma variedade específica, quando contaminada por uma determinada bactéria, pode se tornar contaminada por uma toxina potente: o ácido bongkrek.
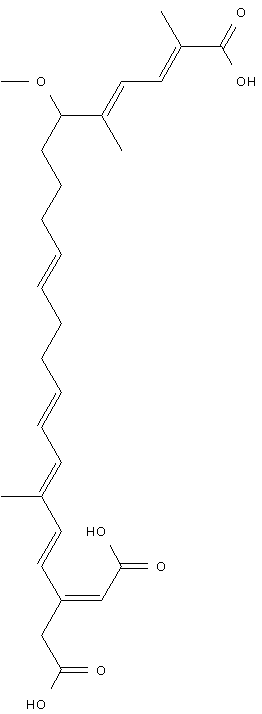
O ácido bongkrek, como o dinitrofenol e o cianeto, é um veneno para a mitocôndria.
http://scienceblogs.com/moleculeoftheday/2007/11/bongkrek_acid_funny_name_unfun.php
Original (English) content from Molecule of the Day (http://scienceblogs.com/moleculeoftheday). Content translated with permission, but portuguese text not reviewed by the original author. Please do not distribute beyond this site without permission from both author and translator.
Vareniclina / Chantix (parar de fumar)
Parar de fumar é algo complicado – na maior parte do tempo as pessoas usam terapias de reposição de nicotina (os adesivos, gomas de mascar, etc) ou medicamentos que agem do SNC (como Wellbutrin/Zyban/Bupropion). Nenhum deles funciona muito bem – os fabricantes da molécula apresentada hoje, a Chantix, a consideram uma novidade para alardear quando seus pacientes conseguiram parar de fumar em uma taxa de 44% em 12 semanas (versus 18% para o placebo).
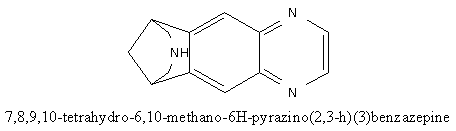
Chantix, contudo, age em um mecanismo diferente, então é ao menos notável. É parcialmente um agonista–antagonista – isto é, ele excita um pouco o receptor pertinente, mas também bloqueia a ação naquele receptor. Neste sentido é como uma metadona para parar de fumar.
http://scienceblogs.com/moleculeoftheday/2007/11/vareniclinechantix_not_like_th.php
Original (English) content from Molecule of the Day (http://scienceblogs.com/moleculeoftheday). Content translated with permission, but portuguese text not reviewed by the original author. Please do not distribute beyond this site without permission from both author and translator.
OBS: os nomes dos medicamentos não foram traduzidos para o português. Não utilize nenhum medicamento sem prescrição médica.
Selenocisteína (selênio em ação)
Os aminoácidos conferem várias funções para as proteínas, e muita química interessante ocorre em poucos resíduos. Muitos resíduos hidrofóbicos como a valina e leucina tem um grande papel – eles não gostam de água, e ajudam a proteína a enovelar; mas a grande parte da catálise ocorre em poucos locais reacionais. Dois destes são a cisteina, e seu irmão raro, selenosisteína.
Indo para baixo na tabela periódica, as coisas ao mesmo tempo mudam e permanecem a mesma. Um cloro age muito como um bromo, que age muito parecido com um iodo, mas existem diferenças distintas em como eles reagem. Só adicionando um traço de iodeto de potássio em algumas reações com um carbono clorado irão apressar as coisas consideravelmente – o iodo é tanto um melhor nucleófilo e um grupo doador se comparado com o cloro.
Descer em um grupo pode ter alguns efeitos bonitos – a serina, que tem um -CH2-OH, é menos reativa do que seu par sulfurado, a cisteína, que tem um -CH2-SH. Continue descendo e você terá a selenocisteína, que tem -CH2-SeH. Um nucleófilo superlativo.
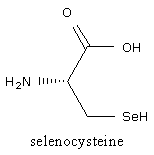
Selênio é raro e fedido, e não encontrará muitas selenoproteínas na natureza. Embora quando você encontra, a evolução terá visto que o selênio tem a sua força – como em sua reação com o composto anti-câncer encontrado no curry, a curcumina.
http://scienceblogs.com/moleculeoftheday/2007/11/selenocysteine_21.php
Original (English) content from Molecule of the Day (http://scienceblogs.com/moleculeoftheday). Content translated with permission, but portuguese text not reviewed by the original author. Please do not distribute beyond this site without permission from both author and translator.
Dinitrato de etilenoglicol (marcando explosivos)
O dinitrato de etilenoglicol é simplesmente um éster dinitrado do etilenoglicol – colocando glicol nas mesmas condições reacionais que resultam nos primeiros explosivos nitro, como nitroglicerina e TNT, resulta neste composto. Porque é importante? Ele tem uma boa pressão de vapor.
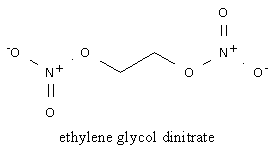
A volatilidade permite que o composto seja detectado por cachorros e outras máquinas que eles usam em aeroportos. Enquanto explosivo, não tem a mesmo poder destrutivo da substância ao qual é misturado. Fabricantes adicionam (e compostos similares, ultimamente) aos seus explosivos como um marcador. Não afeta o desempenho, mas torna mais fácil a detecção. Pense como o caso da mistura de tióis fedidos ao gás natural.
http://scienceblogs.com/moleculeoftheday/2007/11/ethylene_glycol_dinitrate_more.php
Original (English) content from Molecule of the Day (http://scienceblogs.com/moleculeoftheday). Content translated with permission, but portuguese text not reviewed by the original author. Please do not distribute beyond this site without permission from both author and translator.
Luteína (cores para o Halloween)
A luteína é um outro carotenóide – como o retinal, é um terpeno.
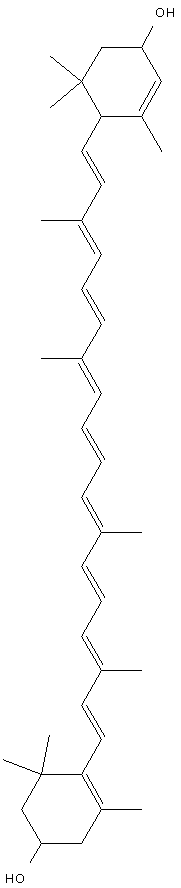
Longa, não é? Aquela cadeia de ligações alternadas duplas e simples resulta em sua maravilhosa cor. Esta, como o retinal, tem seu papel na visão. Sua participação no Halloween é porque é um dos pigmentos encontrados nas abóboras, que as tornam laranjas. Os laranjas brilhantes e cor ferrugem que você vê na natureza tendem a ser graças aos carotenóides.
De fato, quando as folhas estão mudando, você estará vendo os carotenóides mostrando suas cores quando as clorofilas vão embora. Nesta bela imagem abaixo, você pode ver partes da folha perto das veias centrais ainda com sua clorofila, enquanto que as partes um pouco mais longe estão começando a esmaecer e mostrar os carotenóides brilhantes (que estão sempre lá, mas mascarados pela clorofila chamativa!). Existem também, sem dúvida, algumas antocianinas por ali.

http://scienceblogs.com/moleculeoftheday/2007/10/lutein_halloween_carotene.php
Original (English) content from Molecule of the Day (http://scienceblogs.com/moleculeoftheday). Content translated with permission, but portuguese text not reviewed by the original author. Please do not distribute beyond this site without permission from both author and translator.






